
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Роль вирусов в эволюции и медицине
THOMAS HARDTMUTH
Die Rolle der Viren in Evolution und Medizin
Versuch einer systemischen Perspektive
_________________
ТОМАС ХАРДТМУТ
Роль вирусов в эволюции и медицине
Попытка системной перспективы

bdn-steiner.ru
_________________________________________
Перевод: Гончаров Виктор
Вена, 2020
Предисловие
Вопрос о живом всегда был центральным научным вопросом (Schrödinger 1944, Troll 1951, Margulis & Sagan 1995, Ebersbach & al. 2018) и, вероятно, будет всё больше и больше занимать науку в будущем. В частности, для антропософски ориентированного естествознания особым делом, или особой задачей, является наведение моста от вещественно-биохимических к системным наукам о жизни и духовным наукам. В микробиологической области такой мост соединяет то, что мы можем назвать твердыми структурами, такими как мембраны и геномы, с тем, что мы в жидкостно-пластичном называем чистой деятельностью или процессуальностью.
Как каждый мост строится с обеих сторон, так и в устоявшемся естествознании в настоящее время, похоже, возникла сильная тенденция покинуть строго детерминистские и редукционистские позиции[1], - потому что они просто не могут ответить на существенные вопросы, - а вместо этого развивать новые, интегральные и, часто запрашиваемые, трансдисциплинарные способы рассмотрения, - такие как те, с которыми мы сталкиваемся в системно-ориентированных науках о жизни. Это также включает исследования в области биокоммуникации, которые имеют дело с опосредованными знаками взаимодействиями между клетками, клеточными элементами, органами и организмами, в которых молекулярно-биологические, социологические, лингвистические и, наконец, но не в последнюю очередь, эпистемологические и философские аспекты дополняют друг друга.
Основой и поводом для попытки поместить тему о вирусах в духовно-научно ориентированный контекст для автора послужили новаторская и очень тщательно исследованная с научной точки зрения работа австрийского философа и учёного в области биокоммуникаций Гюнтера Витцани (2010)[2] «Биокоммуникация и естественная обработка
генетических текстов»[3], а также текст «Виролюция» английского доктора и эволюционного биолога Фрэнка Райана (2010)[4].
генетических текстов»[5], а также текст «Виролюция» английского доктора и эволюционного биолога Фрэнка Райана (2010)[6].
 ОБ АВТОРЕ
ОБ АВТОРЕ
Доктор медицины Томас Хардтмут, 1956 года рождения, специалист по хирургии и торакальной хирургии, свободный автор, доцент медицинских наук и социальной медицины в дуальном государственном институте Баден-Вюртемберга. Вырос в Хайденхайме, окончил Вальдорфскую школу в 1974 году, изучал медицину в Техническом университете и Мюнхенском университете имени Людвига и Максимилиана (LMU). С 1985 года хирургическая и лечебная деятельность в различных клиниках: больница в Диллингене, университетская клиника в Ульме, клиника в Хайденхайме, где до 2016 года работал главным врачом по хирургии и торакальной хирургии. 1996 — присуждение учёной степени. 1999 - окончание вальдорфского семинара для учителей в Хайденхайме (совместно с работой). Регулярные лекции, семинары и публикации в области медико-антропософских исследований человека. Книжные публикации:
Книжные публикации:
«Сокрытое эго - аспекты понимания ракового заблевания» («Das verborgene Ich – Aspekte zum Verständnis der Krebskrankheit») (Хайденхайм, 2003).
«Заблуждение мысли - дилемма исследования мозга» («Denkfehler – das Dilemma der Hirnforschung») (Heidenheim 2006).
«Сумерки живущих - Предпосылки деменции, депрессии и рака» («In der Dämmerung des Lebendigen – Hintergründe zu Demenz, Depression und Krebs») (Heidenheim 2011).
«Медицина в мёртвой хватке наживы» («Medizin im Würgegriff des Profits») (Heidenheim 2017).
Различные статьи по биологии, иммунологии, неврологии и доклады о путешествиях в журнале «die Drei» (см. http://diedrei.org/autoren-anzeigen/autor/hardtmuth-thomas.html).
Medizin im Würgegriff des Profits (Heidenheim 2017). Diverse Artikel zur Biologie, Immunologie, Neurologie und Reiseberichte in der Zeitschrift »die Drei« (siehe http://diedrei.org/autoren-anzeigen/autor/hardtmuth-thomas.html).
Введение
До идентификации в середине 19 века бактерий и других микроорганизмов в медицинской мысли использовался восходящий к Гиппократу термин «миазмы». Под ним понимались ядовитые пары из почвы, а также вызывающее болезни и заразное загрязнение воздуха и воды в результате гнилостных процессов. Обозначение малярия (mal = плохой, aria = воздух), например, восходит к этому воззрению. Миазма означала не только вещественное зло, но также применялась к духовно-эмоциональному уровню в смысле загрязненной и плохой атмосферы в самом широком смысле. Термин «вирус» (лат. «яд») впервые был использован римским энциклопедистом и врачом-писателем Авлом Корнелием Цельсом в первом веке до нашей эры, на основании того опыта, что при бешенстве передается ядовитая слюна. Этот взгляд на вирусы как на вызывающие болезни «ядовитые существа», в основном сохраняется и по сей день; метафора вируса также используется в переносном смысле для обозначения вредоносной программы на «зараженном» компьютере.
Вообще, ещё преобладает мнение, что вирусы следует рассматривать только как паразитов; благодаря современным процессам секвенирования генома[7] можно проследить генеалогические деревья, или пути эволюционного развития и распространения вирусов, благодаря чему, наше предыдущее понимание вирусов должно быть полностью переписано, и мы должны назначить вирусам роль, которая в смысле системной биологии и медицины выходит далеко за рамки процесса болезни.
Недавние исследования всё более и более четко показывают, что существенные компоненты, если не самые основные компоненты нашего генома, имеют вирусное происхождение, и что вирусы как мобильные генетические медиаторы всегда играли решающую роль в генетической эволюции. Это также проливает совершенно новый свет на наше понимание «оплодотворения» в смысле инноваций, с одной стороны, и роли инфекций, стресса и болезней как стимуляторов эволюции, с другой.
«Viruses are the unending front of evolution (...) they continue to shape the tra-
jectory of life on the planet, including that of humans»[8]. (Luis P. Villarreal).
Сначала мы представим некоторые основы вирусологии, а затем попробуем дать духовно-научную перспективу.
Вирусы

Рис. 1 Аденовирус, изображение с электронного микроскопа с узнаваемой икосаэдрической структурой (Foto: Graham Colm, Lizenz: Creative Commons Attribution 3.0 Unported,
engl. Wikipedia/Adenovirus)
До сих пор ещё обсуждается вопрос о том, можно ли вообще причислять вирусы (рис.1) к живым существам, потому что у них нет собственной цитоплазмы с органеллами (например, митохондриями и рибосомами) и, следовательно, у них нет собственных метаболических (обмена веществ) функций, и потому, в плане выживания или репликации, они всегда зависят от организма-хозяина.
По сути, вирус состоит из трех компонентов: внутри вируса находится генетический материал; это могут быть одно- или двухцепочечные (ss или ds) элементы РНК или ДНК. Растения в основном содержат одноцепочечные, а грибы двухцепочечные РНК-вирусы, бактерии - двухцепочечные ДНК-вирусы. Сегодня мы знаем около 3600 типов вирусов с около 30 000 подтипов, при этом подавляющее большинство вирусов неизвестны, что также относится и к бактериям. Вирусный геном окружен капсулоподобными белками оболочки, которые мы называем капсидами. Обычно они состоят из идентичных строительных блоков (капсомеров), большинство которых имеют геометрическую структуру; наиболее распространенная симметрия капсида - правильный икосаэдр (двадцать поверхностей, рис. 2). Форма икосаэдра, однако, у иначе идентичных вирусов, может варьироваться. Например, большинство вирусов гепатита В, состоят из 180 капсомеров, но около 20% капсидов содержат 240 капсомеров, что создает иную симметрию, биологическое значение которой еще не выяснено. Количество капсомеров обычно кратно 60, то есть, мельчайшие вирусы (пикорнавирусы) состоят из 60 капсомеров. Таким образом, форма вируса связана с определенным порядком чисел и геометрическими законами.
Капсиды служат инокуляционным материалом (вакциной) и важным транспортным средством для нуклеиновых кислот внутри клеток, поэтому они также используются в генной инженерии. Другие вирусы (например, вирусы гриппа, кори и эпидемического паротита, т. е. свинки) имеют спиральный, т. е. спирально-цилиндрический капсид, вирусы оспы - разновидность смешанной формы икосаэдрической и спиральной, а капсид вирусов ВИЧ 1, например, имеет коническую, конусообразную структуру, (рис. 3), хотя она тоже изменчива. Обращает на себя внимание пентоно-гексонная структура, то есть состав из правильных (зеленых на графике) пятиугольников и шестиугольников, к которым мы ещё вернемся. В целом, эти капсидные структуры относительно изменчивы, мы также говорим о метастабильном состоянии; при входе в клетку форма распадается, и когда вирус покидает клетку, он возникает снова, как, в своего рода, кристаллизации без потребления энергии (самосборка). Эти капсидные структуры относительно свободные, подобные нескольким магнитным шарикам, которые самопроизвольно прикрепляются друг к другу.
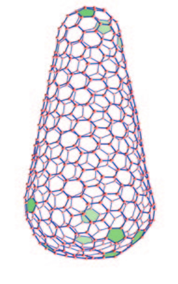

Рис. 2 Рис. 3
Форма Икосаэдра вируса Конический вирус с окрашенной
зелёным пяти- и шестиугольной
структурой
Третий компонент, который, однако, есть не у всех вирусов, - это вирусная оболочка («viral envelope», рис. 4), которая окружает геном и его «упаковку», капсид. Оболочка вируса обычно происходит из биомембраны клетки-хозяина. Когда непокрытый оболочкой вирус покидает клетку или, например, эндоплазматический ретикулум, он захватывает с собой соответствующую пограничную мембрану в качестве отвязывающегося пузырька (рис. 5). Как и все биомембраны, оболочка состоит из двойного липидного слоя, состоящего из оболочечных белков. Оболочка вируса играет важную роль в вирусной иммуногенности и таксономии. Вирусы без оболочки могут покинуть клетку-хозяина, только уничтожив (лизируя) её. Оболочечные вирусы могут делать это без растворения клетки путем экзоцитоза; то есть, вирус высвобождается из интактной (неповреждённой) клетки.
Примечательно, что такие вирусы без оболочки, которые обнаруживаются только среди некоторых вирусов растений, таких как вирус табачной мозаики, могут кристаллизоваться (рис. 6). В противном случае мы знаем такие явления только в неживой природы; когда идентичные молекулярные строительные блоки накладываются друг на друга, возникают такие кристаллоподобные геометрические тела. Самыми известными из них являются снежные кристаллы во всём их многообразии и ледяные цветы, которые связаны с кластерной структурой молекул воды. Вирусы вне своего хозяина или вне контекста жизни в этом отношении ведут себя как неодушевленные вещества.
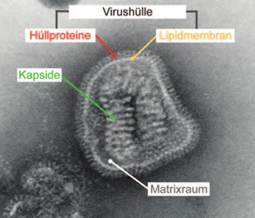
Рис. 4
Вирус гриппа в оболочке
Foto: Centers for Disease
Control and Prevention,
United States Department
of Health and Human-Serv-
ices; Foto-Beschriftung: Gle-
iberg. Lizenzfreies Bild, Wi-
kipedia/Virushülle)
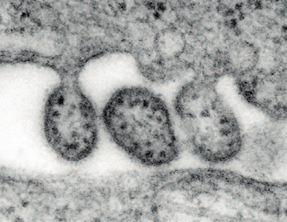 Рис. 5
Рис. 5
Формирование вирусной
оболочки из клеточной
мембраны
Foto: Centers for Disease
Control and Prevention,
United States Department
of Health and Human Ser-
vices, C. S. Goldsmith. Li-
zenzfreies Bild, Wikipe-
dia/Lassafieber)
 Рис. 6
Рис. 6
Вирус табачной мозаики,
кристаллизованный
(Foto: T. Moravec,
lizenzfreies Bild,
Wikipedia/
Tabakmosaikvirus)
Существуют также так называемые вироиды, которые не имеют ни капсида, ни вирусной оболочки и состоят только из кольцевой цепи РНК; они играют роль в патологии растений, но также обнаруживаются в кишечнике человека. Часто бывают подвержены заражению культурные растения, такие как виноград, помидоры и картофель, при этом вспышка реальной болезни во многом зависит от условий окружающей среды.
Отдельные вирусы вне клетки называются вирионами. Самые большие вирионы обычно имеют размер самых мелких бактерий[9], от 15 до 440 нанометров. Вирусы заселяют все без исключения клетки и ткани живой природы; в зависимости от организма-хозяина мы говорим о бактериофагах, заселяющих бактерии, фитовирусах у растений, анимальные вирусы у животных и гуман-вирусы у людей.
Выживание вируса вне его хозяина зависит от структуры его оболочки, от света (УФ-свет повреждает геном вируса) и от температуры; вирус гриппа выживает в воздухе при комнатной температуре около часа, вирус ВИЧ от СПИДа - всего несколько минут. В воде вирусы могут оставаться заразными до 3 недель, во льду - гораздо дольше. В 2014 году из вечной мерзлоты в Сибири были изолированы живые, т. е. инфекционные гигавирусы (питовирусы), возраст которых радиоуглеродным методом был установлен в 30 000 лет. Со своими 700 нм они больше, чем некоторые бактерии (Legendre 2015). К гигавирусам мы ещё вернёмся ниже.
Важно, что вирусы развёртывают своё бытие, или своё специфическое действие, только в связи с их конкретным хозяином, т. е. они обычно экстремально зависят от среды обитания. Это можно пояснить сравнением; если мы вставим небольшой текстовый модуль из научного журнала в любовный роман, то он останется бессмысленным инородным телом, которое не может раскрыть никакого значения или действия в контексте романа, или, как выразился Фрэнк Райан:
«Инъекция вируса в полностью чужеродный организм эквивалентна попаданию совершенно незащищенных людей на Марс» (Ryan 2010: 16)
Подобно тому, как незащищенный человек на Марсе немедленно умирает, вирусы в организмах, не являющихся хозяевами, обычно немедленно уничтожаются иммунной системой. В большинстве случаев вирусы атакуют только определенные типы тканей, такие как риновирусы, которые заселяют слизистую оболочку носа при насморке, или некоторые вирусы герпеса, заселяющие только нервные клетки. В случае СПИДа вирус иммунодефицита человека ( HI-Virus) проникает во весь организм через кровоток, но, так сказать, принимается только Т-лимфоцитами; только здесь он вступает в действие. Чтобы вообще иметь возможность развиваться, вирусы должны иметь коэволюционные отношения со своим организмом-хозяином или родственными организмами-хозяевами. Эволюционные генеалогические деревья вирусов и млекопитающих демонстрируют сильные корреляции, поэтому вирусы, вместе с их организмами-хозяевами, развиваются в очень определённых средах обитания.
Хотя вирусы могут распространяться в воздухе, воде и почве, они всё же остаются функционально связанными со своими организмами-хозяевами. Они являются частью организма, но не связанной с ним напрямую пространственно.
Вирус, меняющий хозяина, часто становится агрессивным. Предполагается, например, что столь опасный для человеческого организма вирус иммунодефицита человека (HI-Virus) изначально происходит от шимпанзе и горилл (SIV, вирус иммунодефицита обезьян), где он не вызывает никаких симптомов болезни.
Передача генетического материала - от горизонтального переноса генов бактерий до оплодотворения млекопитающих - возможна только между живыми существами родственных видов и родов. Поэтому важно подчеркнуть, что большинство патогенных вирусов, а также других возбудителей болезней, передаются человеку от высоко развитых животных. То, что является «нормальным» в организме животного, может, очевидно, стать патологическим в человеке. Возникает даже вопрос, не происходит ли передача патогенов от низших к более высокоразвитым видам в принципе[10]. Вирусы распространены повсеместно, они встречаются везде, где мы имеем дело с жизненными процессами. Каждый грамм салата, который мы съедаем, содержит около миллиарда вирусов[11]. Один миллилитр морской воды содержит 1 миллион бактерий и от 10 до 100 раз больше вирусов[12], а также бесчисленное количество вирусных частиц и фрагментов РНК, о функциях которых в системном контексте нам почти ничего не известно. Цифры в земле еще больше. «Как показывает филогенетический анализ, практически все организмы всех царств организмов инфицированы вирусами или плотно заселены ими, причем с самого начала жизни» (Witzany 2010: 135). Так же и о происхождении вирусов в настоящее время мы можем только предполагать. В принципе, существует две теории: одна рассматривает вирусы как обособленный от живых существ генетический материал, другая рассматривает вирусы как остатки так называемого мира РНК, доклеточной фазы в начале жизни. Луис Вильярреал (Luis Villarreal) однажды сказал в этой связи, что эксперты, придерживающиеся гипотезы о том, что вирусы заимствовали свой генетический материал из геномов хозяев и, таким образом, происходят из геномов хозяев, упустили важную истину о вирусах. А именно, лучше зная геномы вирусов, вы заметите, что подавляющее большинство их генов не встречается ни у животных, ни у растений, ни у бактерий. 90% геномов вирусов не выказывают никаких родственных связей с известными последовательностями генов (Mölling 2015), т. е. это новые вирусы со своими собственными свойствами!
«Это означает, что вирусы могут создавать собственные сложные гены. По большей части они собраны из кусочков, которые в основном происходят от других вирусов. Мировой океан полон таких вирусов. Что я хочу этим сказать: здесь генетическая креативность проявляется в большом масштабе; мы находимся в эпицентре большого первичного биологического взрыва». (Луис Вильярреал, цитата из Райана 2010: 104).
Таким образом, вирусы - это гены в жидко-пластичном состоянии, которые также обладают высокой степенью изменчивости. Если мы сравним скорость мутации клеток человеческого тела, бактерий и вирусов, то в единицу времени вирусы мутируют, грубо говоря, примерно в 1000 раз чаще, чем бактерии, которые, в свою очередь, мутируют в 1000 раз чаще, чем клетки человека. Вирусы, таким образом, меняются генетически примерно в миллион раз быстрее, чем клетки нашего тела. Можно также сказать, что у вирусов очень высокий эволюционный темп. Из исследований СПИДа мы знаем, что ВИЧ (вирус иммунодефицита человека) во время так называемой латентной фазы (фаза без болезней или симптомов после заражения ВИЧ, которая может длиться до 30 лет) мутирует с "захватывающей дух скоростью", так что через 2–3 года исходный штамм уже нельзя будет выделить среди миллионов различных конкурирующих потомков» (Ryan 2010: 60). В зависимости от организма-хозяина, или системной внутренней среды, они видоизменяются, адаптируются и начинают себя чувствовать, в некотором роде, «как дома» в индивидуальном организме. Таким образом, как и при ежегодном гриппе, существуют очень разные штаммы вирусов СПИДа, с разными путями распространения, что объясняет различное течение СПИДа в Африке и США. Изменчивость, или генетическая нестабильность, многих вирусов также является причиной того, что до сих пор не существует вакцины против СПИДа. Лекарственная терапия СПИДа также напоминает борьбу с гидрой, где новые головы гидры соответствуют мутантам вируса. Штамм может мутировать в течение 2 месяцев и, таким образом, стать устойчивым к соответствующему медикаменту.
Как мы увидим ниже, вирусы как носители генетической информации, или информационные посредники, очень пластичны и гено- и фенотипически сильно зависят от контекста, т. е. их поведение и их патогенность даже в большей степени, чем у бактерий, зависят от экологического контекста, то есть, состояния организма и его окружающей ситуации.
Ретровирусы
Ретровирусы, к которым принадлежат также возбудителя СПИДа, представляют собой одноцепочечные оболочечные РНК-вирусы, которые характеризуются тем, что их генетическая информация, с помощью специального фермента (обратной транскриптазы), переписывается в ДНК генома хозяина и, благодаря этому, множится с каждым клеточным циклом. При таких инфекциях мы говорим об экзогенных ретровирусах. Если эти ретровирусы попадают непосредственно в зародышевую линию, они не только передаются как так называемые эндогенные ретровирусы (HERV = humane endogene Retroviren = человеческие эндогенные ретровирусы) с каждым клеточным делением, но и наследуются и остаются неотъемлемой частью генома вида[13] (рис.7). Ретровирусы населяют почти все без исключения животные организмы. С точки зрения биологической эволюции ретровирусы очень старые, их возраст, по меньшей мере, 250 миллионов лет, но, вероятно, даже намного старше. Согласно этому, обратная транскрипция будет одним из старейших генетических процессов, возникших в мире РНК. В новейшее время она была обнаружена у всех организмов (растений, животных, бактерий, архей, эукариот, фагов), даже там, где не встречаются ретровирусы.
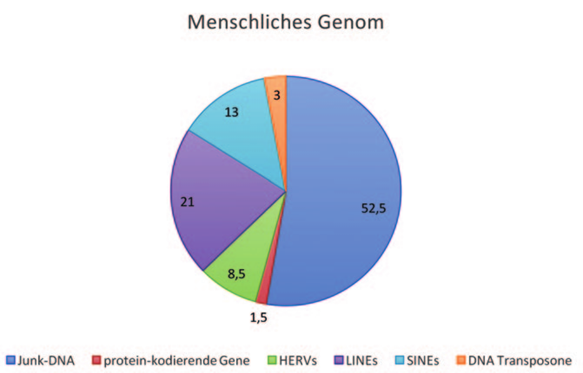
HERV = эндогенные ретровирусы человека, LINEs = длинные вкрапленные ядерные элементы,
SINE = короткие вкрапленные ядерные элементы, дальнейшее объяснение см. в тексте.
(Графика: Томас Хардтмут)
Между тем, в геноме человека описано 31 семейство ретровирусов, что можно проследить до десятков тысяч инфекций зародышевой линии (Villarreal 2004). Райан исходит из того, что ни один геном так сильно не населён эндогенными ретровирусами, как геном человека. Первоначально предполагалось, что интегрированные вирусы будут мутировать в течение поколений и постепенно терять свою активность. Однако теперь мы знаем, что эти, ставшие «оседлыми», ретровирусы передают хозяину фенотипические свойства.
«Как выяснилось в последние годы, инфекционные, очень опасные последствия вирусных инфекций являются, своего рода, особыми случаями и характеризуют те вирусы, которые не могут вести постоянный оседлый образ жизни в организме хозяина. В большинстве случаев вирусы живут в организме хозяина и помогают ему бороться с конкурирующими паразитами (за счет чего достигается более высокий уровень иммунитета, примечание Т. Хардтмута). Таким образом, они часто становятся частью эволюционной истории организма-хозяина, или всего вида-хозяина. Оседлые вирусы имеют решающее значение для разнообразия видов и редактирования генома хозяина. Практически все компетенции естественного редактирования генома, как они представлены в консервации считывания, транскрипции, трансляции и рекомбинации генов (со всеми их этапами и промежуточными этапами), происходят от вирусных способностей. (...) С тех пор, как посредством множества наблюдений стало ясно, что вирусы способны интегрировать генетический материал в геном хозяина, стало ясно и то, что вирусы, наряду с инфекционными жизненными стратегиями, ведут также симбиотический и симбиогенный образ жизни. Они передают хозяину фенотипические свойства, которых нет у неинфицированного хозяина того же вида. Как эндосимбиотические вирусы, которые зависят от репликации хозяина, они являются частью истории хозяина, поскольку они становятся наследуемыми и, таким образом, становятся частью геномной идентичности хозяина. Это документально подтверждено, например, в 10-тысячных случаях инфицирования генома человека эндогенными ретровирусами (Villarreal 2004) (...).
Два разных образа жизни вирусов не являются чистой противоположностью, а в большинстве случаев могут стать частью симбиотического процесса. Он начинается с заражения вирусом. Тогда в инфицированном хозяине может возникнуть равновесие, при котором иммунная система хозяина больше не борется с вирусом, а контролирует его размножение без опасных последствий для хозяина. Оседлый образ жизни сохраняется на протяжении большей части жизни хозяина, но может вернуться к опасному образу жизни, например, когда иммунная система хозяина испытывает стресс. В большинстве случаев эта оседлая вирусная интеграция происходит в организме хозяина за счёт взаимной нейтрализации токсических свойств. Весь спектр модулей зависимости от яда/антидота, которые мы находим во всех генетических текстах во всей живой природе, скорее всего, вирусного происхождения »(Witzany 2010: 121)
Появляется даже всё больше свидетельств того, что эукариотическое[14] ядро и его геном можно проследить до инфекции, вызванной вирусом с двухцепочечной ДНК (Bell 2001, 2006).
Упомянутые модули зависимости от яда/антидота, таким образом, соответствуют потенциальной токсичности, которая контролируется иммунными функциями и функциями гомеостаза организма, и регрессирует в патогенную форму только в случае раздражения системы (стресса), но в непатогенном, системно-интегрированном модусе, представляет собой фенотипическое нововведение. Приходит мысли о кризисе как о возможности развития в самом широком смысле. Как всё новое и чужеродное, которое мы принимаем из окружающей среды, вирус также должен быть распознан обработан и интегрирован. Вся наша иммунная система не только сформировалась в борьбе с вирусами, все защитные функции состоят из интернализованных вирусов! (Mölling 2015).
Мы можем проиллюстрировать это другим примером: в течение своей жизни человек создаёт свой собственный совершенно индивидуальный микробиом, к которому принадлежат бесчисленные бактерии, вирусы и другие микроорганизмы, которые он принимает из внешнего мира и делает частью своей собственной физиологии. Теперь мы упомянули о двойственной природе этих «иммигрантов»: с одной стороны, они могут вызывать у нас болезни как, так называемые, возбудители, патогены, но они также могут интегрироваться в организм в качестве партнеров и перенять там выполнение определенных задач. В такой амфибиоз у человека входит, например, Helicobacter pylori, бактерия, которая много тысячелетий населяла человеческие желудки, и которую всё еще можно обнаружить в желудках большинства людей в начале 20 века. После того, как было установлено, что носители Helicobacter pylori имеют более высокий риск развития язвы желудка и рака желудка, эти коренные жители, с помощью специальных антибиотиков, были истреблены. Только 6% людей, родившихся после 1995 года, имеют в себе его зачаток. Однако теперь очевидна обратная сторона; без него резко возрастает риск рака пищевода и особенно также бронхиальной астмы. Эта связь доказана многими исследованиями (Blaser 2017: 142 ff.). Это показывает, что Helicobacter играет, как раз, важную роль в регуляции кислоты в желудке и, следовательно, является важным симбионтом, который развивает патогенные свойства только при раздражении системы. Вирусы и бактерии в организме человека имеют двойную природу: их патогенная форма зависит от состояния организма и окружающей его среды. Например, вирус Эпштейна-Барра (ВЭБ) вызывает у людей в западном мире относительно безвредную железистую лихорадку Пфайффера (мононуклеоз), зато в Африке - злокачественное заболевание лимфатических узлов (лимфома Беркитта), а в Китае - рак горла.
Наш геном большей частью построен из эндогенных ретровирусов. Этот факт проливает полностью новый свет на наше понимание болезни. Излеченная болезнь - это больше, чем иммунобиологическое событие. Да, эти интегрированные вирусы защищают нас от нового инфицирования родственными конкурирующими вирусами. Но это только одна сторона медали. Каждое преодоленное заболевание также имеет эволюционный аспект, поскольку оно не только увеличивает нашу иммунологическую компетентность, но также означает проделанный опыт в самом широком смысле для человека в целом. Такой процесс обучения имеет генетический отпечаток на клеточном уровне, - будет интересно посмотреть, что эпигенетика выявит в будущем, - но для онтогенеза человека на протяжении всей жизни эти генетические следы имеют гораздо более широкий горизонт важности.
Гигавирусы
Только недавно открытые гигавирусы представляют собой революцию в современной вирусологии: эти организмы представляют собой переходную форму между вирусами и бактериями и поэтому чрезвычайно полезны для нашего понимания эволюции. Они больше, чем многие бактерии, и имеют до 2500 генов (Pandoravirus). У вирусов обычно от 10 до 100 генов. Причина, по которой крупные вирусы так долго оставались не обнаруженными, заключалась в простой методологической и технической проблеме: для выделения и исследования вирусов использовались фильтры для удаления бактерий из образца, при этом гигавирусы также удалялись и таким образом систематически ускользали от наблюдения. Теперь мы обнаруживаем их повсюду, в море, в пресной воде, даже в кишечнике человека, и они обладают удивительными свойствами: они содержат строительные блоки для биосинтеза белка, что ранее было исключительной привилегией одноклеточных организмов. Гигавирусы могут поглощать другие вирусы (вирофаги), с которыми они обмениваются своим генетическим материалом. Их часто обнаруживают у водорослей (фикоднавирусов), плотность популяции которых они регулируют, как фаги делают это у бактерий. Меловые скалы возле Рюгена и на южном побережье Англии являются результатом деятельности гигавирусов, потому что они лизируют (растворяют) известковые водоросли в море, осаждая при этом образующийся карбонат кальция.
Амёбы также являются популярным организмом-хозяином для гигантских вирусов. Амёбы - это фагоциты, сравнимые с макрофагами в организме человека, и поэтому содержат много генетического материала различного происхождения. Пандора-вирусы используют это, так что их геном содержит странную смесь в значительной степени неизвестных нуклеотидных последовательностей - отсюда и название. Для 93% пандора-генов нет гомологий в базах данных генов, что является загадкой для исследования: «Это напоминание о том, что наша перепись микробного разнообразия еще далека от завершения» (Philippe & al. 2013).
Значение гигавирусов, возрастом примерно 2,7 миллиарда лет, для нашего понимания эволюции заключается в том, что их можно рассматривать как связующее звено между фактически неодушевленным миром вирусов и метаболически активными прокариотами.
ДНК и РНК - Эргон и Энергея
Если мы распределим генетический материал в нашем организме между двумя полюсами в соответствии с критериями, с одной стороны, стабильности, надёжности, прочности и, с другой стороны, нестабильности, гибкости, пластичности, живости, тогда мы можем отнести ДНК ближе к стабильному полюсу, а РНК - к живому, гибкому полюсу. Говоря по Аристотелю, ДНК соответствует эргону (Ergon), т. е. статике, а РНК энергии (Energeia) - активной деятельности. Можно также сказать, что РНК воплощает в себе больше становящееся, а ДНК - ставшее. У эукариотов и всех высших живых существ РНК, как накопитель информации (Speichermedium), играет второстепенную роль, скорее, она оказывается посредником генетической эволюции.
В отличие от, в значительной степени, жесткой структуры ДНК, РНК представляет собой очень вариабельную и полифункциональную молекулу, которая не только считывает генетическую информацию с ДНК (транскрипция) и передает ее рибосомам для производства белка (трансляции), но также самыми разными способами модифицирует, регулирует и под контролирует эти процессы. РНК является не только носителем информации, она также обладает ферментативными свойствами (рибозимы[15]), она может автокаталитически реплицироваться (размножаться) и «обрабатывать» себя.
«Нестабильность РНК является необходимой предпосылкой для высокой продуктивности различных последовательностей РНК с их быстрой адаптируемостью, то есть, также и для большого разнообразия различных идентичностей РНК» (Witzany 2010: 189).
К этим обрабатывающим элементам принадлежат также, так называемые, сплайсосомы[16], катализаторы экспрессии гена, состоящие из комплекса РНК/белок, которые вырезают некодирующие интроны от пре-РНК и связывают кодирующие участки (экзоны). Мы говорим об альтернативном сплайсинге, когда сплайсосома вырезает различные экзоны из одного и того же набора генетических данных и собирает их вместе в новом порядке таким образом, чтобы можно было произвести большое количество различных белков. Благодаря этому становится понятным, почему человек может производить сотни тысяч различных белков со своим относительно скромным количеством кодирующих генов. Не количество генов, а сплайсосома и другие мобильные генетические элементы, способствуют генетическому разнообразию и комплексности. 80% элементов РНК имеют период полураспада менее 2 минут, остальные - около 5-10 минут (Baudrimont & al. 2017); таким образом, они являются очень мимолётными элементами, которые возникают и исчезают очень быстро с минимальными затратами энергии, в отличие от относительно прочной ДНК, которая, как известно, остаётся сохранённой, по крайней мере фрагментами, через тысячи лет после смерти[17]. Скорость репликации РНК примерно от одного до десяти миллионов раз выше, чем у ДНК-геномов (McClure 2000). Мы знаем (пока) только 13 различных классов РНК, включая только сотни микроРНК (miR), которые выполняют такие некодирующие функции и взаимодействуют в очень сложной сети связанных регуляторных элементов - «весь набор инструментов естественной генной инженерии» (Дж. А. Шапиро), описание которых здесь выходит за рамки[18]. Множество различных элементов РНК создают впечатление охватываемой взглядом системы, но, в конечном итоге, они отражают только то из реальных процессов, что мы в состоянии расшифровать на снимке. Жидко-пластичная, взаимосвязанная с окружающей средой динамика в целом, описана этим быть ещё не может.
«Нет гомогенной РНК, нет определённого вида, а есть только смесь различных РНК с разными последовательностями: некая масса, которая привел к появлению термина, придуманного Манфредом Эйгеном (Manfred Eigen): квазивиды (Quasispezies). Высокая частота мутаций молекул РНК во время репликации приводит не к конкретной молекуле, а к квазивидам, состоящим из множества мутантов. Эта смесь по-прежнему вызывает проблемы с РНК-содержащими вирусами, такими как ВИЧ и грипп. Существует не один вирус, а совокупность различных секвенций (последовательностей)» (Mölling 2015, курсив: Th. H.)
Современные методы секвенирования генома показали нечто такое, что имеет решающее значение для понимания: а именно, что все эти некодирующие РНК-агенты, а также мобильные элементы ДНК (SINEs, LINEs, LTRs, non LTRs), включая сплайсосомы, имеют вирусное происхождение, - одно, наверное, из самых важных научных открытий последних десятилетий! Малые РНК также играют роль в эпигенетике, например, когда они обрабатывают гистоны, носители негеномного наследования (см. ниже).
Таким образом, ДНК более точно соответствует фиксированному наследию эволюции: при этом только около 1,5–2% генома являются стабильными, кодирующими белок, элементами. Подавляющее большинство генома человека состоит из некодирующих повторяющихся последовательностей («мусорной» ДНК), значение которых еще не совсем понятно. В прошлом считалось, что речь идёт о «генетических отходах», которые будто бы откладывались в процессе эволюции. Однако эта теория не оказалась слишком просветляющей, поскольку больше нигде в природе не сохраняются безфункциональные отходы. Исследования последних лет показали (Villarreal 2005) скорее то, что некодирующие последовательности в основном обладают более высокими контрольными (управляющими) функциями и происходят из ретровирусной РНК.
Следовательно, большая часть нашего генетического материала восходит к интеграции вирусов в ходе эволюции. Ср
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|