
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Практическое занятие № 11.. Неорганическая химия.. Решение задач.. Задание для самоподготовки.. I. Расчеты по уравнению реакции.. Алгоритм.. Примеры решения задач. II. Вычисление массовой доли вещества, находящегося в растворе в %.. Алгоритм.
Практическое занятие № 11.
Тема 3.2.
Неорганическая химия.
Решение задач.
1. Задание для самоподготовки.
Самостоятельно ознакомиться с методиками решения задач.
I. Расчеты по уравнению реакции.
Алгоритм.
1) Составьте краткое условие задачи.
2) Составьте уравнение реакции, расставьте коэффициенты.
3) Определяем вещества которые потребуются для расчета и находим их молярные массы по периодической таблице.
4) Подпишите над формулами веществ известные величины( массу или объем), неизвестную обозначьте как х.
5) Под формулами записываем величины соответсвующие уравнению реакции.
6) Найдите неизвестную величину(массу или объем), используя метод пропорции.
Примеры решения задач
1. Вычислить массу гидроксида кальция полученного, если в реакцию с водой, взятой в избытке, вступило 11,2 г оксида кальция?
| Дано: m(CaO) = 11,2 г | Решение 11,2 х CaO + H2O = Ca(OH)2 56 74 M(CaO) = 40 + 16 = 56 г/моль M (Ca(OH)2) = 40 + (16 +1) ∙2 = 74 г/моль |
| Найти: m(Ca(OH)2 - ? | 
 Ответ: m(Ca(OH)2 =14,8 г.
Ответ: m(Ca(OH)2 =14,8 г.
|
2. Сколько грамм ортофосфорной кислоты можно получить при нагревании 28,4 г оксида фосфора (V) с водой?
| Дано: m(P2O5) = 28,4 г | Решение 28,4 х P2O5 + 3H2O = 2H3PO4 142 98 ∙ 2 M(P2O5) = 31∙ 2 + 16 ∙ 5 = 142 г/моль M (H3PO4) = 1 ∙ 3 + 31 + 16 ∙ 4 = 98 г/моль |
| Найти: m(H3PO4) - ? | 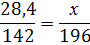
 Ответ: m(H3PO4) =39,2 г.
Ответ: m(H3PO4) =39,2 г.
|
II. Вычисление массовой доли вещества, находящегося в растворе в %.
Алгоритм.
1. Составьте краткое условие задачи.
2. Рассчитать массовую долю вещества находящегося в растворе по формуле
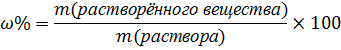
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|