
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Записать всё в тетрадь для работ!
27/11/20г. УРОК № 49,50
Тема: Соли и их свойства
Смотреть по ссылке: https://www.youtube.com/watch?v=7_4eo0FKbjk
! Записать всё в тетрадь для работ!
Образование солей
Приведем наиболее важные из них.
1. Взаимодействие кислот с основаниями (реакция нейтрализации):
NаОН + НNO3 = NаNO3 + Н2О
Al(OH)3 + 3НС1 = AlCl3 + 3Н2О
2. Взаимодействие металлов с кислотами:
Fе + 2HCl = FeCl2 + Н2
Zn + Н2SО4 разб.= ZnSO4 + Н2
3. Взаимодействие кислот с основными и амфотерными оксидами:
СuO + Н2SO4 = СuSO4 + Н2О
ZnO + 2HCl = ZnСl2 + Н2О
4. Взаимодействие кислот с солями:
FeCl2 + H2S = FeS↓ + 2HCl
AgNO3 + HCI = AgCl↓ + HNO3
Ba(NO3)2 + H2SO4 = BaSO4↓ + 2HNO3
5. Взаимодействие растворов двух различных солей:
BaCl2 + Na2SO4 = ВаSO4↓ + 2NаСl
Pb(NO3)2 + 2NaCl = РbС12↓ + 2NaNO3
6. Взаимодействие оснований с кислотными оксидами (щелочей с амфотерными оксидами):
Са(ОН)2 + СО2 = СаСО3↓ + Н2О,
2NаОН(тв.) + ZnO 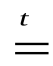 Na2ZnO2 + Н2О
Na2ZnO2 + Н2О
7. Взаимодействие основных оксидов с кислотными:
СаO + SiO2 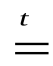 СаSiO3
Na2O + SO3 = Na2SO4 СаSiO3
Na2O + SO3 = Na2SO4
| 8. Взаимодействие металлов с неметаллами:
2К + С12 = 2КС1
Fе + S 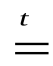 FеS FеS
|
| 9. Взаимодействие металлов с солями. Cu + Hg(NO3)2 = Hg + Cu(NO3)2 Pb(NO3)2 + Zn = Рb + Zn(NO3)2 10. Взаимодействие растворов щелочей с растворами солей CuCl2 + 2NaOH = Cu(OH)2↓+ 2NaCl NaHCO3 + NaOH = Na2CO3+ H2O | 11.Получение двойных солей: КОН + 2NaOH + H3PO4 = KNa2PO4 + 3H2O двойной фосфат калия и натрия K2O + 2Na2O + 2H3PO4 = 2KNa2PO4 + 3H2O 3Mg + 3Zn + 4H3PO4 = Mg3Zn3(PO4)4 + 6H2 двойной фосфат магния и цинка K2CO3 + 2Na2CO3 + 2H3PO4 = 2KNa2PO4 + 3H2O + 3CO2 |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|