
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Жёсткость воды. Устранение жёсткости воды.
Жёсткость воды. Устранение жёсткости воды.
Учебник, параграф 9.
1) Анализ так называемой жёсткой воды показывает наличие большого количества ионов магния
(Mg2+) и кальция(Ca2+).Как они попадают в раствор?
Давайте вспомним, какими свойствами обладают кальций и магний и их соединения: (переписать цепочки превращений и составить следующие превращения):
А) Са⟶CaO⟶гидроксид кальция⟶карбонат кальция⟶гидрокарбонат кальция;
Б)Mg⟶гидроксид магния⟶карбонат магния⟶гидрокарбонат магния⟶карбонат магния.
Какие минералы, содержащие эти элементы, вам известны? (Подписать названия всех веществ в цепочках).
2) Природная вода, протекая в земле, соприкасается с различными минералами и горными породами и растворяет некоторые составляющие их вещества.
Но вы можете мне возразить и сказать, что некоторые соединения нерастворимы.
Дело в том, что помимо обычного растворения, вода, содержащая в себе углекислый газ, оказывает на некоторые минералы химическое действие, превращая карбонаты в гидрокарбонаты, растворимые в воде. Поэтому ключевая вода содержит значительноеколичество ионов кальция имагния. Именно такая вода называется жёсткой.
3)Записать определение жёсткой воды из учебника.
4) Какая жёсткость называется временной, а какая – постоянной? (найти ответ в учебнике).
5) По величине жесткости природную воду делят на:
А) мягкуюж < 80 мг/л (дождевая вода)
Б) средней жесткости ж = 80 – 160 мг/л
В) жесткую ж = 160 – 240 мг/л
Г) очень жесткуюж > 240 мг/л (морская вода)
6) В жесткой воде увеличивается расход мыла и порошка при стирке белья, медленно разваривается
мясо и овощи, снижается моторика желудка. Жесткая вода непригодна для систем водоснабжения
и питания водонагревательной техники. Жёсткая вода при умывании сушит кожу, в ней плохо
образуется пена при использовании мыла. Использование жёсткой воды вызывает появление осадка (накипи) на стенках котлов, в трубах и т. п.
В то же время, использование слишком мягкой воды может приводить к коррозии труб, так как, в этом случае отсутствует кислотно-щелочнаябуферность, которую обеспечивает гидрокарбонатная (временная) жёсткость.
Потребление жёсткой или мягкой воды обычно не является опасным для здоровья, хотя есть данные о том, что высокая жёсткость способствует образованию мочевых камней, а низкая — незначительно увеличивает риск сердечно-сосудистых заболеваний.
Жёсткость природных вод может варьироваться в довольно широких пределах и в течение годанепостоянна. Увеличивается жёсткость из-за испарения воды, уменьшается в сезон дождей, а также в период таяния снега и льда.
7) Почему же в жёсткой воде мыло не пенится? (Ответ найдите в учебнике и запишите в тетрадь).
8) Способы устранения жёсткости (прочитайте теоретическую часть и результаты оформите в виде таблицы:
| Виды жёсткости | Соли, обуславливающие жёсткость воды | Способы её устранения | Уравнения реакции |
Временная жесткость (карбонатная) обусловлена присутствием в воде гидрокарбонатов Са(НСО3)2 и Mg(НСО3)2. Карбонатную жесткость легко устранить кипячением воды, прикотором Са2+ и Mg2+ удаляются образуя нерастворимые осадки:
Са(НСО3)2 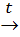 CаСО3↓ + СО2↑ + Н2О
CаСО3↓ + СО2↑ + Н2О
Уравнение с гидрокарбонатом магния записать самостоятельно.
Для уменьшения карбонатной жесткости применяется метод известкования, при котором в
обрабатываемую воду вводят известь Са(ОН)2. Реакции, протекающие при введении извести, можно записать в молекулярной форме:
Са(НСО3)2 + Са(ОН)2 → 2СаСО3↓ + Н2О
Mg(НСО3)2 + Са(ОН)2 → Mg(ОН)2↓ + 2СаСО3 + Н2О
Постоянная жесткость (неустранимая или некарбонатная) сохраняется при кипячении воды, поскольку постоянная жесткость обусловлена присутствием в воде сульфатов, хлоридов и других солей Са и Mg (запишите эти соли в таблицу). Для снижения некарбонатнойжесткости обычно используют кальцинированную соду (Na2CO3):
MgSO4 + Na2CO3 → MgCO3↓ + Na2SO4
(Самостоятельно запишите уравнения реакции снижения некарбонатной жёсткости для хлорида
магния и кальция).
При одновременном добавлении извести и соды можно избавиться от карбонатной и некарбонатной жесткости (известково-содовый способ).
Современный способ умягчения воды основан на использовании ионно-обменных смол - ионитов (катионитов и анионитов). Катиониты – это синтетические ионно-обменные смолы – алюмосиликаты, например:Na2[Al2Si2O8 ∙ nH2O].
Оформить данную работу и прислать мне на почту до следующего урока.
Присылают ученики: Кнорр Елена, Копытин Кирилл, Моисеенко Олег, Сотников Данил, Тенячкин Иван, Чигошвили Андрей.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|