
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Выполненные работы отправляете на электронную почту строго 16.04. Ранее отправленные работы будут перенаправлены в раздел «СПАМ»
Проверочная работа №3
Тема урока: «Соли азотной кислоты. Разложение нитратов»
Рабочий материал:
1. Учебник, параграфы: «Азот. Аммиак. Кислородсодержащие соединения азота»
2. Видеоролики: «Вступление» и «Основная часть. Соли азотной кислоты» - https://vk.com/id590336507 Natalya Bernje
3. Платформа «ЯКласс»: предмет «Химия», глава VIII, п.6 «Азот и его соединения» → «Соли аммония. Нитраты»
Выполненные работы отправляете на электронную почту строго 16.04. Ранее отправленные работы будут перенаправлены в раздел «СПАМ»
План работы:
1. Посмотрите видеоролики: «Вступление» и «Основная часть»
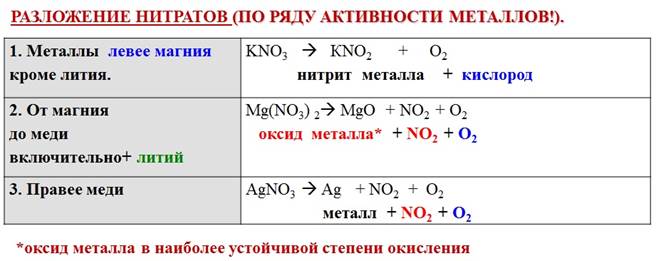
2. Напишите тему урока и перепишите в тетрадь справочный материал (см. ниже: таблица «Разложение нитратов»)
3. Напишите реакции разложения и уравняйте методом электронного баланса: нитрат лития, нитрат бария, нитрат ртути, нитрат никеля
4. Ответьте на вопрос: ниже написаны три реакции – «разложение нитрата аммония». Подумайте, почему в зависимости от температуры получаются разные продукты реакции, проанализируйте
Выполненное домашнее задание (фото) нужно выслать на эл. почту в форме word или pdf (nbernje@yandex.ru) с обязательной пометкой (фамилия, имя, класс)
Справочный материал для заданий №2,3

Справочный материал для задания №4
Нитрат и нитрит аммония:
Нитрат аммония разлагается в зависимости от температуры так:
NH4NO3 = N2O ↑+ 2H2O (190-245°C)
2NH4NO3 = N2↑ + 2NO + 4H2O (250-300°C)
2NH4NO3 = 2N2 ↑+ O2 + 4H2O (выше 300°C)
Нитрит аммония:
NH4NO2 = N2 ↑+ 2H2O
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|