
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Домашнее задание № 02 (Термодинамика. Газовые законы)
Домашнее задание № 02 (Термодинамика. Газовые законы)
10 класс, 2015-2016 уч.г.
1. Найти формулу некоторого соединения углерода с водородом, если известно, что 0,65 г этого вещества в газообразном состоянии создаёт в объёме 1 дм3 при температуре 27 °С давление 105 Па.
2. Найти формулу некоторого соединения углерода с водородом, если известно, что 1 г этого вещества в газообразном состоянии создаёт в объёме 1 дм3 при температуре 27 °С давление 5,6-104 Па.
3. Шаровая молния представляет собой слабо светящийся газовый шар, свободно плавающий в воздухе. Согласно одной из моделей, молния состоит из идеального газа, представляющего собой комплексное соединение, каждая молекула которого состоит из иона азота (m = 14), связанного с несколькими молекулами воды (m = 18). Температура молнии t = 600 °С. Температура окружающего воздуха t0 = 20 °. Сколько молекул воды связывает каждый ион азота?
4. В горизонтально расположенном теплопроводящем цилиндре под подвижным поршнем заперт воздух при атмосферном давлении и комнатной температуре. В объём под поршнем впрыснули m=5 г легко испаряющейся жидкости. После того, как жидкость испарилась, оказалось, что объём, занятый воздухом и парами жидкости, увеличился на ΔV = 0,6 л. Найти по этим данным молярную массу жидкости. Наружное давление равно атмосферному, t=27 °С. Объёмом, занимаемым жидкостью в начале опыта можно пренебречь.
5. Некоторая масса водорода занимает объём V1 = 1 м3 при давлении Р1 = 2105 Па и температуре T1 = 250 К. Какое давление Р2 будет иметь та же масса водорода при температуре T2 = 5000 К в объёме V2 = 10 3, если при столь высокой температуре молекулы водорода полностью диссоциируют на атомы?
6. В сосуде находится 4 г молекулярного водорода при температуре T1 = 300 К и давлении Р1 = 105 Па. При повышении температуры до T2 = 3000 К происходит частичная диссоциация молекул водорода и давление возрастает в 15 раз. Какая часть молекул водорода диссоциировала на атомы?
7. В сосуде объёма V = 1 дм3 находится m = 0,28 г азота. Азот нагрет до температуры t = 1500 °С. При этой температуре а = 30% молекул азота диссоциировало на атомы. Определить давление в сосуде.
8. В сосуде объемом 67 л находится кислород при нормальных условиях. При повышении температуры до 2700 °С одна треть молекул кислорода диссоциирует на атомы. Какое давление будет при этом в сосуде?
9. В сосуде находится смесь азота и водорода. При температуре Т, когда азот полностью диссоциировал на атомы, а диссоциацией водорода ещё можно пренебречь, давление в сосуде равно Р. При температуре 2Т, когда оба газа полностью диссоциировали, давление в сосуде равно 3Р. Каково отношение чисел атомов азота и водорода в смеси.
10. В сосуде постоянного объёма находятся 1 моль неона и 2 моля водорода. При температуре T1=300К, когда весь водород молекулярный, давление в сосуде 105 Па. При температуре Т2 К=3000 К давление возросло до 1,5×106 Па. Какая часть молекул водорода диссоциировала на атомы?
11. В объёме V0 при температуре T и давлении Р находился воздух, содержащий некоторое количество озона О3. После долгого выдерживания в тени озон полностью превратился в молекулярный кислород. При том же давлении температура воздуха стала Т, объём – V. Найдите начальное число молей озона.
12. В сосуде объёма V = 1 дм3 находится m = 0,2 г углекислого газа. При температуре T = 2600 К некоторая часть молекул С02 диссоциировала на молекулы окиси углерода и кислорода: С02 - СО + О2. При этом давление в сосуде оказалось равным Р = 108 кПа. Найти степень диссоциации СО2 при этих условиях.
13. Серный ангидрид SO3 в количестве n1=1 моль поместили в замкнутый сосуд и нагрели до температуры Т1=1000 К, при которой он частично диссоциирует на сернистый ангидрид (SO2) и кислород (О2). Степень диссоциации в этих условиях оказалась α1=0,2 (т.е. 20% от первоначально имевшихся молекул SO3 распались на SO2 и О2). Когда в тот же сосуд поместили n2=0,4 моля SO3, то для получения такого же, как в первом опыте, давления, газ пришлось нагреть до температуры Т2=2000К. Определите степень α2 диссоциации SO3 во втором опыте.
14. В замкнутый сосуд поместили n1 = 1 моль четырёхокиси азота N2O4. При этом произошла частичная её диссоциация на двуокись согласно реакции N2O4 = 2NO2. Степень диссоциации оказалась равной α1 = 0,2 (т. е. 20% первоначально имевшихся молекул четырёхокиси распались на двуокись). В сосуде установилось давление Р1 = 2,4×104 Па. Когда в тот же сосуд поместили n2 = 0,5 моля четырёхокиси, после установления равновесия при той же температуре, что и в первом опыте, давление оказалось равным Р2 = 1,25×104 Па. Определить степень α2 диссоциации N2O4 во втором опыте.
15. Внутри закрытого с обоих концов горизонтально расположенного цилиндра имеется поршень, который скользит в цилиндре без трения. С одной стороны поршня находится m1=3 г водорода, а с другой m2=14 г азота. Какую часть объёма цилиндра занимает водород.
16. Вертикально расположенный цилиндр, закрытый с обеих сторон, разделён тяжёлым теплонепроницаемым поршнем на две части; обе части сосуда содержат одинаковое количество воздуха. При одинаковой температуре воздуха в обеих частях Т1=400К давления в нижней части вдвое больше давления в верхней части. До какой температуры надо нагреть воздух в нижней части сосуда, чтобы объёмы верней и нижней частей стали одинаковыми.
17. В вертикально расположенном цилиндре сечения S под поршнем массы m находится воздух. На поршне лежит груз. Когда груз с поршня убрали, объём, занимаемый воздухом под поршнем, вдвое возрос, а температура этого воздуха вдвое уменьшилась. Определить массу груза M. Атмосферное давление равно Р0.
18. Цилиндрический сосуд сечения S = 10 см2 закрыт массивным поршнем. При подъёме сосуда с ускорением 2g объём газа под поршнем уменьшается в 1,5 раза. Найти массу поршня, считая температуру газа постоянной. Внешнее давление Р0 = 105 Па.
19. Цилиндрический сосуд сечения S = 10 см2 закрыт поршнем массы m = 5 кг. При движении сосуда вниз с ускорением 4g объём газа под поршнем увеличился в 2 раза. Температура газа не изменилась. Найти внешнее давление.
20. Цилиндрический сосуд длиной L = 1,5 м, разделенный лёгким теплонепроницаемым поршнем, заполнен идеальным газом. В начальном состоянии объём левой части сосуда вдвое больше правой, а температуры в обеих частях одинаковы. Насколько переместится поршень, если температуру в правой части увеличить вдвое? Температура в левой части поддерживается постоянной.
21. В левой части цилиндрического сосуда длиной L = 1 м, разделенного теплонепроницаемым поршнем, находится водород, а в правой — гелий. Объём гелия в 3 раза больше объёма водорода. При нагревании гелия поршень сместился на l = 5 см. На сколько градусов изменилась температура гелия, если начальные температуры газов были одинаковы? Температура водорода поддерживается постоянной и равной 350 К.
22. Вертикально расположенный цилиндр разделён на две равные части тяжёлым теплонепроницаемым поршнем, который может скользить без трения. В верхней половине цилиндра находится водород при температуре T и давлении Р, в нижней части – кислород при температуре 2T. Цилиндр перевернули вверх дном. Чтобы поршень по-прежнему делил цилиндр на равные части, пришлось охладить кислород до температуры Т/2. Температура водорода осталась прежней (Т). Определить давление кислорода в первом и втором случаях.
23. Цилиндр разделён на две части теплоизолирующим поршнем, связанным с каждым днищем пружиной. Вначале азот, заполняющий левую часть цилиндра, и гелий, заполняющий правую часть цилиндра, находятся при одинаковой температуре Т. При этом поршень делит цилиндр пополам, а обе пружины находятся в ненапряжённом состоянии. Когда азот нагрели до температуры Т1, он занял ¾ цилиндра. При какой температуре Т2 азот займёт 7/8 длины цилиндра.
24. В цилиндрическом сосуде с вертикальными гладкими стенками и открытой в атмосферу верхней частью под подвижным тяжёлым поршнем находится n молей идеального газа. К поршню и дну сосуда прикреплена пружина с жёсткостью k. При температуре газа T1 пружина растянута и её длина равна L. До какой температуры T2 надо нагреть газ, чтобы его объём увеличился в 2 раза?
25. Сосуд, заполненный смесью водорода и гелия, отделён от равного ему по объёму пустого сосуда полупроницаемой перегородкой, свободно пропускающей молекулы гелия и непроницаемой для водорода. После установления равновесия давление в первом сосуде упало на 10%. Определить отношение масс гелия и водорода. Температура поддерживалась постоянной.
26. Одинаковые по массе количества водорода и гелия поместили в сосуд объёма VI, который отделён от пустого сосуда объёма V2 полупроницаемой перегородкой, свободно пропускающей молекулы водорода и непроницаемой для гелия. После установления равновесия давление в первом сосуде упало в 2 раза. Определить V2/V1. Температура постоянна.
27.  В сосуде длины L, разделённом на три части лёгкими поршнями, находятся водород, азот и гелий. Материал, из которого изготовлен левый поршень, оказался проницаем для водорода и гелия. Правый поршень проницаем только для водорода. Найти смещения поршней после установления равновесия в системе. Первоначальные давления и температуры газов одинаковы. Объём, занимаемый водородом, больше объёмов азота и гелия в два раза.
В сосуде длины L, разделённом на три части лёгкими поршнями, находятся водород, азот и гелий. Материал, из которого изготовлен левый поршень, оказался проницаем для водорода и гелия. Правый поршень проницаем только для водорода. Найти смещения поршней после установления равновесия в системе. Первоначальные давления и температуры газов одинаковы. Объём, занимаемый водородом, больше объёмов азота и гелия в два раза.
28. 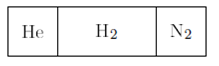 Сосуд длины L разделён лёгкими подвижными поршнями на три части, в которых находятся гелий, водород и азот. Левый поршень проницаем для водорода и гелия, а правый — только для водорода. Начальные давления газов одинаковы, начальный объём водорода вдвое больше начальных объёмов гелия и азота, а температура гелия вдвое больше начальных температур водорода и азота. Найти смещения поршней от начального положения после окончания процесса диффузии.
Сосуд длины L разделён лёгкими подвижными поршнями на три части, в которых находятся гелий, водород и азот. Левый поршень проницаем для водорода и гелия, а правый — только для водорода. Начальные давления газов одинаковы, начальный объём водорода вдвое больше начальных объёмов гелия и азота, а температура гелия вдвое больше начальных температур водорода и азота. Найти смещения поршней от начального положения после окончания процесса диффузии.
29. В горизонтально расположенной трубке столбиком ртути длиной l = 12 см заперт слой воздуха толщиной L = 35 см. Если трубку повернуть один раз открытым концом вниз, а другой раз вверх, то столбик ртути смещается. Разность величин этих смещений от начального горизонтального положения равна 2 см. Найдите величину наружного давления (в мм ртутного столба).
30. В вертикально расположенной тонкой трубке длиной 3L=840 мм с открытым в атмосферу верхним концом, столбиком ртути длиной L = 280 мм заперт мой воздуха длиной L. Какой максимальной длины слой ртути можно долить сверху в трубку, чтобы она из трубки не выливалась? Внешнее давление Ро = 770 мм рт. ст.
Ответы
1. СН4.
2. СО2.
3. 4.
4. 208 г.
5. 8×105 Па.
6. ½.
7. 190 кПа.
8. 14,5 атм.
9. 1:2.
10. ¾.
11. 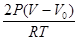 .
.
12. 20%.
13. 75%.
14. 0,25.
15. ¾.
16. 700 К.
17. 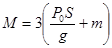 .
.
18. 10/3 кг.
19. 3,5 атм.
20. 25 см.
21. 100.
22. 8P/5, 2P/5.
23. 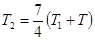 .
.
24. 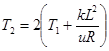 .
.
25. ½.
26. 3.
27. L/2; L/4.
28. Правый – 5L/12, левый – нельзя определить.
29. 720 мм.
30. 350 мм.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|