
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Признаки цепных реакций
Цепными реакциями называется реакции, протекающие с участием химически активных частиц (свободные атомы и радикалы) и состоящие из большого количества повторяющихся стадий. К цепным реакциям относятся реакции горения, медленного окисления, радиоактивного распада, передачи нервного импульса, ядерные реакции и т.д.
К характерным особенностям цепных реакций относятся:
1) скорость реакции не совпадает со скоростью, вычисленной по теории активных соударений, т.е. Wнаблюдаемая >> Wрасчета;
2) исключительная чувствительность к примесям положительных и отрицательных катализаторов, которые ускоряют или замедляют реакцию;
3) зависимость скорости реакции от размеров, формы, материалов сосуда. В сосуде большего объема скорость реакции больше. Скорость реакции замедляется, если в свободное пространство поместить осколки кварца, стекла, фарфора и т.п.
4) Наличие нижнего и верхнего пределов воспламенения или взрыва для реакций окисления газов, ниже и выше которых реакции идут медленно или вообще не идут.
Особенности протекания этих реакций объясняется цепным механизмом реакции, в разработку которого существенный вклад был внесен академиком Н.Н. Семеновым (рис. 5.6). Активная частица “А”, образовавшаяся путем столкновения или любым другим путем, может дезактивироваться, но может дать промежуточное вещество “Z”, которое в свою очередь может разложиться без образования продуктов или дать продукты реакции и новую активную частицу. При этом, активация одной молекулы исходных веществ приводит к образованию большого количества молекул продуктов реакции.
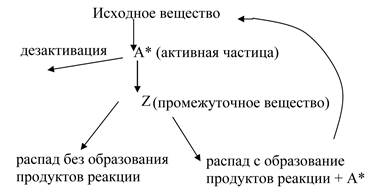
Схема цепной реакции
Основные положения теории цепных реакций:
1) в реакции участвуют атомы или свободные радикалы (частицы, имеющие не спаренный электрон). Атом или свободный радикал обладают исключительной активностью по отношению к валентно-насыщенной молекуле;
2) при взаимодействии валентно-насыщенной молекулы с атомом или свободным радикалом “свободная валентность” не исчезает, а дает начало новой активной частице (принцип неучтожимости свободной валентности).
Под “свободной валентностью” надо понимать частицы, имеющие неспаренный электрон (атом или свободный радикал).
Основные стадии цепной реакции:
1) зарождение цепи - элементарная стадия цепной реакции, приводящая к образованию свободной валентности из валентно-насыщенной молекулы;
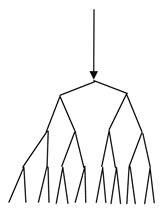
Рис. 7. Схема разветвленной реакции.
Пример разветвленной реакции - синтез воды при высокой температуре.
2H2 + O2 = 2H2O
1. Зарождение цепи: H2 + O2 = 2OH˙,
OH˙+ H2 = H2O + H˙
2. Развитие цепи: H˙+ O2 = OH˙ + Ö (бирадикал)
Ö + H2 = OH˙ + H˙,
H˙+ O2 + Н2 = 2OH˙ + H˙ -стадия развития цепи.
Из одной активной частицы получается несколько, каждая из которых дает начало своей цепи.
3. Обрыв цепи: 2H˙ = H2
2ÓH = H2O2
Признаки цепных реакций
· Реакция ускоряется в присутствии инициаторов, причём распад одной молекулы инициатора приводит к превращению нескольких молекул реагирующих веществ.
· Реакция инициируется при действии света или ионизирующего излучения, причём квантовый выход больше 1.
· Реакция тормозится ингибиторами, а скорость расхода ингибитора гораздо меньше скорости неингибированной реакции.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|