
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Соли -сложные вещества, состоящие из атомов металлов (иногда входит водород или гидроксильная группа) и кислотных остатков.
Соли -сложные вещества, состоящие из атомов металлов (иногда входит водород или гидроксильная группа) и кислотных остатков.

Классификация солей
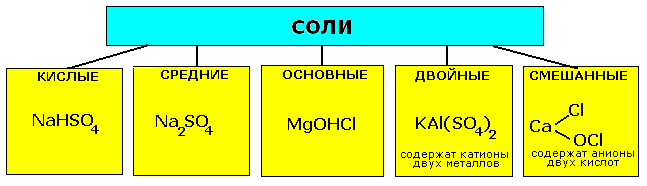
| СРЕДНИЕ | КИСЛЫЕ | ОСНОВНЫЕ | ДВОЙНЫЕ | СМЕША ННЫЕ | КОМПЛЕК СНЫЕ |
| Na2SO4 | NaHSO4 | Mg(OH)Cl | K2NaPO4 | Ca-OCl │ Cl | Na[Al(OH)4] |
Чаще всего мы будем работать со средними солями:
Названия солей
для средней соли -
название кислотного остатка + название металла + указываем валентность для металла с переменной валентностью
Na2SO4- сульфат натрия,
CuSO4- сульфат меди (II)
для кислой соли –
«гидро» или «дигидро» + название кислотного остатка + название металла + указываем валентность для металла с переменной валентностью
NaHSO4 – гидросульфат натрия;
NaH2PO4 – дигидроортофосфат натрия
для основной соли –
«гидроксо» + название кислотного остатка + название металла + указываем валентность для металла с переменной валентностью
Mg(OH)Cl-гидроксохлорид магния
ПОЛУЧЕНИЕ
1. Из металлов:
металл + неметалл = соль
Fe + S = FeS
металл (металлы до Н2) + кислота (р-р) = соль + Н2
Zn +2 HCl = ZnCl2 + H2
Металл1 + соль1 = металл2 + соль2
ВИДЕО "ВЗАИМОДЕЙСТВИЕ МЕТАЛЛОВ С СОЛЯМИ"
Примечание: (металл2 стоит в ряду активности правее)
 Fe + CuCl2 = FeCl2 + Cu
Fe + CuCl2 = FeCl2 + Cu
|
| 2.Из оксидов: кислотный оксид + щелочь = соль + вода SO3 + 2 NaOH = Na2SO4 + H2O основный оксид + кислота = соль + вода CuO + H2SO4 = CuSO4 + H2O основный оксид + кислотный оксид = соль Na2O + CO2 = Na2CO3 |
| 3. Реакция нейтрализации: кислота + основание = соль + вода HCl + NaOH = NaCl + H2O |
| 4. Из солей: соль1 + соль2 = соль3 + соль4↓ NaCl + AgNO3 = NaNO3 +AgCl ↓ соль1 + щелочь = нерастворимое основание + соль 2 CuSO4 + 2NaOH = Cu(OH)2 ↓+ Na2SO4 соль1 + кислота1 = кислота2 + соль2 2NaCl + H2SO4 = 2HCl + Na2SO4 Примечание: Все реакции обмена протекают до конца, если одно из образующихся веществ нерастворимо в воде (осадок), газ или вода. |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|