
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Практическая работа «Решение расчетных задач»
Практическая работа «Решение расчетных задач»
1 вариант
1. Рассчитать массовые доли элементов в молекуле
C6H12O6
w(C) = ? w(H) = ? w(O) = ?
2. Приведена формула вещества состава CxHyOz. Зная массовые доли элементов, определите его молекулярную формулу
w(C) = 36,5% w(H) = 15% w(O) = 48,5%
3. В 110 г. воды растворены 52 г. соли хлорида калия. Рассчитайте массовую долю соли в растворе.
4. Расставьте коэффициенты в уравнении реакции
Fe + H2O = H2↑ + Fe2O3
5. 
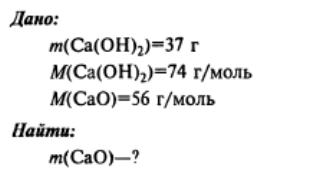
Примечание: для решения задачи необходимо составить уравнение реакции
Практическая работа «Решение расчетных задач»
2 вариант
1. Рассчитать массовые доли элементов в молекуле
K2Cr2O7
w(K) = ? w(Cr) = ? w(O) = ?
2. Приведена формула вещества состава CxHyOz. Зная массовые доли элементов, определите его молекулярную формулу
w(C) = 24% w(H) = 12% w(O) = 64%
3. Определите массовую долю некоторой соли в растворе, приготовленном из 10,07 г. соли и 190,12 г. воды.
4. Расставьте коэффициенты в уравнении реакции
HNO3 = H2O+NO2+O2
5. 
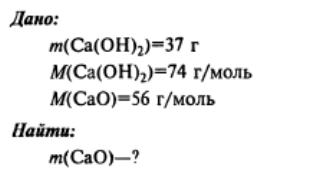
Примечание: для решения задачи необходимо составить уравнение реакции
Практическая работа «Решение расчетных задач»
3 вариант
1. Рассчитать массовые доли элементов в молекуле
H3PO4
w(H) = ? w(P) = ? w(O) = ?
2. Приведена формула вещества состава CxHyOz. Зная массовые доли элементов, определите его молекулярную формулу
w(C) = 24% w(H) = 12% w(O) = 64%
3. Определить массовую долю растворенного вещества хлорида натрия в растворе, полученном растворением 15 г. NaCl в 235 г. воды.
4. Расставьте коэффициенты в уравнении реакции
Fe(OH)2+H2O+O2 = Fe(OH)3
5. 
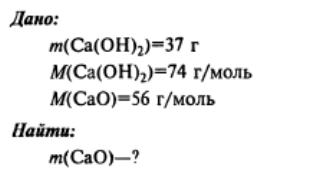
Примечание: для решения задачи необходимо составить уравнение реакции
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|