
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Тема: Электролиз водных растворов
ПГС-19-1 14.05.2020 Лаб зан. № 14 (4 пара) Химия
Тема: Электролиз водных растворов
По теме лабор. занятия следует знать материал Вложения 1. Обратите внимание на законы Фарадея 1 и 2, знать формулы для каждой формулировки закона Фарадея (в случае необходимости, использовать рекомендуемую литературу по курсу «Химия»). Законы Фарадея используются при решении задач по электролизу. Электролиз применяется для нанесения металлических покрытий, например, для цинкования, меднения и др.
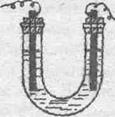
Опыт 1. Электролиз раствора серной кислоты с медным анодом.
Для выполнения опыта используется электролизер →
Налейте в электролизер около 3/4 объема 1 М раствора серной кислоты Н2SO4. Погрузите т угольный и медный электроды. Угольный электрод соедините с отрицательным полюсом источника тока − с катодом (К−); медный - с положительным полюсом ,с анодом (А+). На электродах происходят реакции:
· на катоде процесс восстановления 2Н+ + 2е → Н2. Что наблюдаете на катоде?
· на медном аноде происходит растворение меди: Сu0 – 2е → Cn2+.
При образовании ионов Cn2+ раствор у анода становится голубым.
Ответить письменно на вопросы(в тетради для лабор. работ):
1. Что называется электролизом? Из чего состоит электролизер (установка)?
2. Напишите процессы при электролизе расплава хлорида магния MgCl2. Вычислите массу образующегося магния на катоде (в результате процесса восстановления), если через расплав проходил ток силой 2 А в течение 1,5 часов. Вычисления сделать по закону Фарадея.
Прошу сдать отчеты по лаб. работе 14 с ответами на вопросы к 19 мая (выслать через старосту для проверки к зачету). Теорию выучить. С уважением, Елена Николаевна
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|