
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Информационная карточка. Соединения водорода»
Прочитайте информационную карточку «Соединения водорода».
Используя полученную информацию, разгадайте кроссворд.
По вертикали: планета, на которой есть «водородный лед».
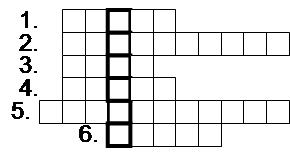
По горизонтали:
1. Физическое свойство, по которому можно отличить аммиак от остальных веществ.
2. Газ, из которого образуется угольная кислота.
3. Физическое свойство фосфорной кислоты, используемое человеком.
4. Вещество, в состав которого входят углерод и водород.
5. Яд.
6. Вещество, после горения которого образуется сернистая кислота.
Информационная карточка
«Соединения водорода»
Важнейшими соединениями водорода являются: вода H2O, аммиак NH3, сероводород H2S, метан СН4, кислоты.
Вряд ли все представляют, что такое аммиак. И даже если сообщить, что это бесцветный газ с резким раздражающим запахом, многие не догадаются, что это такое. А вот если напомнить, что раствор аммиака в воде – это нашатырный спирт, всем станет ясно, о каком веществе идет речь.
Метан входит в состав природного газа, используется в бытовых газовых приборах. Он без цвета и запаха, но тем не менее мы легко почувствуем «запах газа» при неисправности конфорки в плите. Дело в том, что при использовании в быту в метан добавляют пахучие примеси, чтобы легко обнаружить утечку СН4: вдыхание природного газа вызывает удушье, а смесь с воздухом взрывоопасна.
С кислотами человек сталкивается ежедневно. Дождевая вода лишь на первый взгляд кажется чистой, без примесей. На самом деле в ней растворено немало веществ. Например, за счет растворения углекислого газа СО2 она является слабым раствором угольной кислоты Н2СО3. раствор угольной кислоты находится в бутылке с лимонадом и другими газированными напитками. Пузырьки в них не что иное, как СО2.
Впрочем, после летней грозы в дождевой воде оказывается еще и азотная кислота HNO3. получается она при растворении в воде оксидов азота, образующихся во время вспышки молний.
В последние десятилетия в дождевой воде стали обнаруживаться заметные примеси серной H2SO4 и сернистой H2SO3 кислот. Они образуются из оксидов серы, выделяющихся при извержении вулканов и сжигании топлива (особенно нефти и каменного угля).
Но вот дождь закончился, засуетились насекомые. И тут не обойтись без кислот: некоторые жуки-бомбардиры в момент опасности «стреляют» парами серной кислоты, муравьи для защиты используют муравьиную кислоту. Значит, кислоты могут вырабатываться в организме?
В желудке человека содержится соляная кислота HCl. Она помогает перевариванию белков пищи. Кроме того, она – сильный бактерицид, - большинство бактерий, попавших с пищей, погибает под действием соляной кислоты. Так что врачи не случайно тревожатся, если у пациента пониженная кислотность желудочного сока, и заставляют его пить слабый раствор соляной кислоты.
Немало кислот в нашей пище. Очень приятной на вкус является разбавленная фосфорная кислота Н3РО4. Небольшие ее добавки в мармелад и сиропы улучшают вкусовые качества, кроме того, фосфорная кислота необходима нервным клеткам головного мозга.
А вот сероводородная кислота H2S обеспечивает запах протухших белковых продуктов (мяса, яиц, рыбы). Кстати, сероводород является ядом. Пожалуй, нет такого газа, который убивал так быстро живое существо. Человек, сделавший один вдох чистого HS, внезапно теряет сознание и падает мертвым из-за паралича дыхательного центра.
И еще с одной кислотой вы легко встретились бы лет пять назад. Если бы вам понадобилось склеить два листка бумаги, то незаменимым оказался бы конторский или силикатный клей – раствор кремниевой кислоты H2SiO3.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|