
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Рассмотреть таблицу, повторить свойства оксидов, кислот, оснований (растворимых и нерастворимых), солей. Перенести таблицу в тетрадь.
Задание 1. Рассмотреть химические свойства солей, переписать их аккуратно в рабочую тетрадь (под формулой каждого вещества написать его название) и ВЫУЧИТЬ!!!
Химические свойства солей
1). Соль + кислота → другая соль + другая кислота (↓ или ↑)
Важно! Должен образоваться либо осадок либо газ
Na2SiO3 + 2HNO3 = 2NaNO3 + H2SiO3↓
K2SO3 + 2HCl = 2KCl + H2SO3 (H2O + SO2↑)
2). Растворимая соль + растворимое основание (щелочь) → другая соль + нерастворимое основание (осадок↓)
Cu(NO3)2 + 2NaOH = 2NaNO3 + Cu(OH)2↓ 2FeCl3 + 3Ba(OH)2 = 3BaCl2 + 2Fe(OH)3↓
3). Растворимая соль 1 + растворимая соль 2 → нерастворимая соль (осадок↓) 3 + растворимая соль 4
Важно! Должен образоваться осадок!
Pb(NO3)2 + K2S = PbS↓+ 2KNO3 СaCl2 + Na2CO3 = CaCO3↓ + 2NaCl
4). Растворимая соль металла(1) + металл(2) = соль металла (2) + металл (1)
Zn + CuSO4 = ZnSO4 + Cu Cu + 2AgNO3 = Cu(NO3)2 + 2Ag
Важно:
- Ме(2) должен находиться в ряду активности металлов левее металла(1)
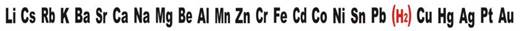
|
Задание 2.Запишите уравнения возможных реакций. Дайте название всем веществам. Определите тип каждой реакции.
1) Fe(NO3)2 + NaOH =
2) K2CO3 + HNO3 =
3) Ba(NO3)2 + K2SO4 =
4) ZnCl2 + Mg =
5) Na2SO4 + Al =
6) CuSO4 + LiOH=
7) PbS + KNO3 =
8) CrBr3 + H3PO4 =
Рассмотреть таблицу, повторить свойства оксидов, кислот, оснований (растворимых и нерастворимых), солей. Перенести таблицу в тетрадь.
Таблица «Химические свойства основных классов неорганических соединений»
| Основный оксид | Кислотный оксид | Кислота | Основание | Соль | |
| Металл | Соль + H2↑ | Соль + Ме | |||
| Н2О | Основание | Кислота | |||
| Основный оксид | Соль | Соль + Н2О | |||
| Кислотный оксид | Соль | Соль + Н2О | |||
| Кислота | Соль + Н2О | Соль + Н2О | Соль + Кислота (↓ или ↑) | ||
| Основание | Соль + Н2О | Соль + Н2О | Соль + Основание (↓) | ||
| Соль | Соль + Кислота (↓ или ↑) | Соль + Основание (↓) | Соль + Соль (↓) |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|