
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Контрольная работа
Контрольная работа
Распределение по вариантам:
11 А
| Абрамов Никита | ||
| Алифанова Светлана | ||
| Анучина Анжелика | ||
| Белявский Никита | ||
| Беляева Александра | ||
| Бондаренко Анна | ||
| Грядушкина Дарья | ||
| Дремина Мария | ||
| Елагин Кирилл | ||
| Завалина Екатерина | ||
| Иванникова Ангелина | ||
| Капустин Сергей | ||
| Котляренко Екатерина | ||
| Кривенкова Полина | ||
| Малюкова Софья | ||
| Маслова Элла | ||
| Милюкова Виктория | ||
| Некрасов Юрий | ||
| Покидова Лана | ||
| Пономарёва Владлена | ||
| Прокофьева Валерия | ||
| Проходова Алёна | ||
| Сотникова Елена | ||
| Суворова Оксана | ||
| Тепляков Степан | ||
| Трещалина Валерия | ||
| Тучкова Ангелина | ||
| Филонова Ксения | ||
| Хевронина Елена | ||
| Худиев Тимур | ||
| Щеблыкина Алина |
11 Б
| Астапова Анна | ||
| Багайоко София | ||
| Богер Павел | ||
| Будиловский Андрей | ||
| Голубых Вячеслав | ||
| Деревенских Даниил | ||
| Джатенова Амина | ||
| Дубовской Данил | ||
| Зайцева Софья | ||
| Зверев Константин | ||
| Золотова Анастасия | ||
| Иконописцева Олеся | ||
| Кирпичов Владислав | ||
| Китаев Максим | ||
| Копытин Павел | ||
| Кравчук Мария | ||
| Ляпин Данила | ||
| Малыхина Алина | ||
| Минаков Артем | ||
| Новиков Артем | ||
| Привалов Юрий | ||
| Рассман Артем | ||
| Ревина Ульяна | ||
| Савушкина Алина | ||
| Самойлов Владислав | ||
| Свиридов Иван | ||
| Созонова Анна |
11 В
| Быков Максим | ||
| Власов Игорь | ||
| Волченко Сергей | ||
| Дера Артем | ||
| Дубинин Кирилл | ||
| Жданова Алина | ||
| Красюк Максим | ||
| Лапоногов Алексей | ||
| Макаров Степан | ||
| Мещеряков Константин | ||
| Офицеров Владимир | ||
| Полякова Полина | ||
| Разуваев Андрей | ||
| Рябова Екатерина | ||
| Толстых Михаил | ||
| Щеголев Александр | ||
| Яковлев Владимир | ||
| Япринцев Максим |
11 Г
| Адерихин Дмитрий | ||
| Алексеева Арина | ||
| Баев Максим | ||
| Белоусов Даниил | ||
| Бурякова Олеся | ||
| Бушуева Анастасия | ||
| Валуйский Всеволод | ||
| Варлыгин Дмитрий | ||
| Винокурова Александра | ||
| Глазунов Михаил | ||
| Жилина Ирина | ||
| Зайцев Артем | ||
| Иконописцева Алина | ||
| Каширский Андрей | ||
| Миленин Артём | ||
| Нгуен Тхи Нгок | ||
| Пономарева Дарья | ||
| Попов Артем | ||
| Расторгуева Ирина | ||
| Сагань Антон | ||
| Селин Дмитрий | ||
| Синюгина Алина | ||
| Ситников Егор | ||
| Смирнова Виктория | ||
| Тарасов Александр | ||
| Терещенко Елизавета | ||
| Торопцев Павел | ||
| Шабанов Станислав |
Вариант 1
Часть 1
1.Какую электронную конфигурацию имеет самый активный неметалл:
(1) 1s22s22p3 (2)1s22s22p4 (3)1s22s22p6 (4)1s22s22p5.
2.В каком ряду представлены только вещества с ковалентной полярной связью:
(1) Cl2, NH3, HCl (2) HBr, NO, Br2
(3) H2S, H2O, S8 (4) HCl, H2O, PH3
3.Атомную кристаллическую решетку имеет:
(1) алмаз (2) аммиак
(3) хлорид аммония (4) сероводород
4.Низшую степень окисления фосфор проявляет в соединении:
(1) Н3РO4 (2) Р2О3 (3) Р2О5 (4) РН3
5.Только кислоты расположены в ряду:
(1) H2SO4, SO2, NaCl (2) K2S, HNO3, KHS
(3) H3PO4, HI, H2S (4) HCl, KCl, HClO
6.Хлорид железа (II) реагирует с каждым из двух веществ:
(1) MgO и HCl (2) CO2 и HNO3 (3) CaO и CO2 (4) AgNO3 и Zn
7.В схеме превращений
CuCl2 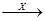 Cu(OH)2
Cu(OH)2 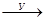 CuCl2
CuCl2
веществами «Х» и «У» являются соответственно:
(1) NaOH и NaCl (2) H2O и HCl (3) NaOH и HCl (4) H2O и NaCl
8.К гомологическому ряду алканов не относится:
(1) 2,3-диметилпентан (2) гексан
(3) гексен-1 (4) 2-метил-3-этилгептан
9.В реакцию 2CO + O2  2CO2 ввели 3 л оксида углерода (II) и 2 л кислорода. Вычислите объем непрореагировавшего газа.
2CO2 ввели 3 л оксида углерода (II) и 2 л кислорода. Вычислите объем непрореагировавшего газа.
Часть 2
1.Установите соответствие между реагирующими исходными веществами и образовавшимися продуктами реакции:
| Исходные вещества | Продукты реакции | |||
CaCO3 + HCl 
| А | CaO + CO | ||
CaCO3 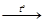
| Б | Na2CO3 + Ca(OH)2 | ||
CaCO3 + NaOH 
| В | CaCl2 + CO2 + Н2О | ||
CaCO3 + NaCl 
| Г | CaO + CO2 | ||
| Д | не взаимодействуют |
2.Установите соответствие между схемой реакции и изменением степени окисления окислителя:
| Схема реакции | Изменение степени окисления окислителя | |||
H2S + Cl2 + H2O  HCl + H2SO4 HCl + H2SO4
| А | 2Cl-  Cl2 Cl2
| ||
KMnO4 + HCl 
 KCl + MnCl2 + Cl2 + H2O KCl + MnCl2 + Cl2 + H2O
| Б | S-2  S+6 S+6
| ||
H2SO3 + Cl2 + H2O   H2SO4 + + HCl H2SO4 + + HCl
| В | O2  2O-2 2O-2
| ||
SO2 + O2  SO3 SO3
| Г | S+4  S+6 S+6
| ||
| Д | Cl2  2Cl- 2Cl-
| |||
| Е | Mn+7  Mn+2 Mn+2
|
Часть 3
Вещество содержит 30,4% N и 69,6% О. Плотность паров этого вещества по азоту равна 3,285. Определите молекулярную формулу вещества.
Вариант 2
Часть 1
1.Наименьший радиус имеет атом с электронной конфигурацией:
(1) 1s22s22p63s23p1 (2)1s22s22p63s23p2
(3)1s22s22p63s23p3 (4)1s22s22p53s23p4.
2.В ряду веществ хлороводород, сульфид натрия, бром, хлорид кальция, этан, оксид углерода (IV) количество веществ с ионной связью равно:
(1) одному 2) двум (3) трем (4) четырем
3.Атомную кристаллическую решетку имеет:
(1) алмаз (2) аммиак
(3) хлорид аммония (4) сероводород
4.Максимальную степень окисления азот проявляет в соединении:
(1) Са3N2 (2) N2О (3) Ca(NO3)2 (4) NaNO2
5.Амфотерными гидроксидами являются:
(1) Ca(OH)2 и NaOH (2) KOH и Fe(OH)3
(3) Be(OH)2 и Al(OН)3 (4) Zn(OH)2 и CsOH
6.Оксид углерода (II) реагирует с:
(1) HCl (2) CuO (3) K2SO4 (4) SO3
7.В схеме превращений Zn 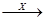 ZnSO4
ZnSO4 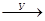 Zn(OН)2
Zn(OН)2
веществами «Х» и «У» являются соответственно:
(1) SO3 и NaOH (2) H2SO4 и NaOH
(3) SO2 и Fe(OH)2 (4) H2SO4 и Mg(OH)2
8.Не является изомером гексана:
(1) гексен-1 (2) 2-метилпентан
(3) 2,2-диметилбутан (4) 2,3-диметилбутан
9.Для получения аммиака в реакцию 3H2 + N2  2NH3
2NH3
ввели 3,3 л водорода и 2 л азота. Вычислите объем образовавшегося аммиака.
Часть 2
1.Установите соответствие между реагирующими исходными веществами и образовавшимися продуктами реакции:
| Исходные вещества | Продукты реакции | |||
AlCl3 + NaOH 
| А | Al2(SO4)3 + HCl | ||
AlCl3 + AgNO3 
| Б | не взаимодействуют | ||
AlCl3 + H2SO4 (раствор) 
| В | AgCl + Al(NO3)3 | ||
AlCl3 + Zn(NO3)2 
| Г | Al(OH)3 + NaCl | ||
| Д | ZnCl2 + Al(NO3)3 |
2.Установите соответствие между схемой реакции и изменением степени окисления восстановителя:
| Схема реакции | Изменение степени окисления восстановителя | |||
Fe2O3 + CO  Fe + CO2 Fe + CO2
| А | Cu0  Cu+2 Cu+2
| ||
Сu + H2SO4  CuSO4 + SO2 + H2O CuSO4 + SO2 + H2O
| Б | Fe+2  Fe+3 Fe+3
| ||
FeCl2 + Cl2  FeCl3 FeCl3
| В | Cl2  2Cl- 2Cl-
| ||
Fe(NO3)2 + Zn  Zn(NO3)2 + Fe Zn(NO3)2 + Fe
| Г | C+2  C+4 C+4
| ||
| Д | Fe+3  Fe+2 Fe+2
| |||
| Е | Zn0  Zn+2 Zn+2
|
Часть 3
Массовая доля углерода в углеводороде составляет 83,33%. Плотность паров этого углеводорода по водороду равна 36. Определите формулу углеводорода.
Вариант 3
Часть 1
1.Элементу, электронная формула которого 1s22s22p53s23p4, соответствует водородное соединение:
(1) HЭ (2) ЭH3 (3) H2Э (4) ЭH4.
2.В каком ряду представлены только вещества с ковалентной неполярной связью:
(1) HCl, O2, CO2 (2) N2, O3, H2
(3) Cu, NaI, H2O (4) CH4, NH3, F2
3.Ионную кристаллическую решетку имеет:
(1) графит (2) бромоводород
(3) железо (4) бромид аммония
4.Минимальную степень окисления сера проявляет в соединении:
(1) K2SO4 (2) Na2SО3 (3) SO2 (4) CaS
5.К солям относится каждое из двух веществ:
(1) КCl и NaHSO3 (2) H2SO3 и Cr(OH)3
(3) NH3 и MgBr2 (4) H2S и CaCO3
6.Могут взаимодействовать друг с другом:
(1) Fe и Ca(OH)2 (2) Al и KNO3 3) Al и NaOH (4) Cu и HCl
7.В схеме превращений Cl2 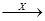 NaCl
NaCl 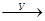 AgCl
AgCl
веществами «Х» и «У» являются соответственно:
(1) NaOH и Ag (2) Na и Ag
(3) Na2SO4 и AgNO3 (4) Na и AgNO3
8.2-метилпентан и гексан являются:
(1) гомологами (2) структурными изомерами
(3) геометрическими изомерами (4) одним и тем же веществом
9.В реакцию 2SO2 + O2  2SO3 ввели 3 л оксида серы (IV) и 2 л кислорода. Вычислите объем непрореагировавшего газа.
2SO3 ввели 3 л оксида серы (IV) и 2 л кислорода. Вычислите объем непрореагировавшего газа.
Часть 2
1. Установите соответствие между реагирующими исходными веществами и образовавшимися продуктами реакции:
| Исходные вещества | Продукты реакции | |||
| MgO + SO2 | А | MgSO3 + H2О | ||
| MgO + SO3 | Б | MgSO4 + H2 | ||
| MgO + H2SO4 | В | MgSO3 | ||
| MgO + H2SO3 | Г | MgSO4 | ||
| Д | MgSO4 + H2O |
2.Установите соответствие между схемой реакции и изменением степени окисления окислителя:
| Схема реакции | Изменение степени окисления окислителя | |||
КМnO4 + HBr  KBr + MnBr2 + H2O KBr + MnBr2 + H2O
| А | Mn+2  Mn+4 Mn+4
| ||
MnCl2 + Zn  ZnCl2 + Mn ZnCl2 + Mn
| Б | Mn+7  Mn+2 Mn+2
| ||
КNO2 + KMnO4 + H2SO4 
 KNO3 + MnSO4 + K2SO4 + H2O KNO3 + MnSO4 + K2SO4 + H2O
| В | Cl2  2Cl- 2Cl-
| ||
MnCl2 + Cl2  MnCl4 MnCl4
| Г | Mn+2  Mn0 Mn0
| ||
| Д | N+3  N+5 N+5
| |||
| Е | Zn  Zn+2 Zn+2
|
Часть 3
Вещество содержит 85,71% С и 14,29% Н. Относительная плотность паров этого вещества по водороду равна 14. Определите молекулярную формулу вещества.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|