
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Промежуточной аттестации по Химии за курс 8 класса.
Промежуточной аттестации по Химии за курс 8 класса.
ученика (цы) 8класса
МБОУ «Погореловская ООШ»
Фамилия __________________________ Имя ______________________ Класс 9
Дата:__20.05.2020г_
Вариант
Часть 1
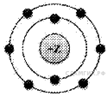 А 1. На приведённом рисунке изображена модель атома химического элемента
А 1. На приведённом рисунке изображена модель атома химического элемента
1) 2-го периода VIIIA группы
2) 2-го периода VIA группы
3) 3-го периода VIA группы
4) 3-го периода VIIIA группы
А 2. В каком ряду химических элементов усиливаются металлические свойства соответствующих им простых веществ?
1) калий → натрий → литий 3) углерод → кремний → германий
2) сурьма → мышьяк → фосфор 4) алюминий → кремний → углерод
А 3. Ковалентная неполярная связь образуется между атомом хлора и атомом
1) углерода 2) калия 3) водорода 4) хлора
А 4. Степень окисления кислорода в гидроксиде натрия равна:
1) - 2 2) + 1 3) + 2 4) 0
А5. В каком ряду расположены сложные вещества?
1) Mg, Al, N2 3) H2SO4, CaO, PH3
2) CO2, Ca, H2O 4) Si, N2, Fe2O3
А 6. Какое уравнение соответствует реакции обмена?
1)CuCl2+Fe=Cu+FeCl2 3)2KOH+H2SO4=K2SO4+2H2O
2)2Al+Fe2O3=2Fe+Al2O3 4)2Na+O2=Na2O2
А 7. Верны ли суждения о правилах применения и опасности для здоровья препаратов бытовой химии?
А. Стиральные порошки нельзя использовать для мытья посуды.
Б. Работать с хлорсодержащими дезинфицирующими средствами следует при плотно закрытой двери в помещении.
1) верно только А 3) верны оба суждения
2) верно только Б 4) оба суждения неверны
А 8. К химическим явлениям относятся:
1.Замерзание воды 2.Измельчение кристаллов сахара
3. испарение воды. 4.гниение пищевых продуктов
А9.При взаимодействии оксида бария с водой образуется:
1.Соль и вода. 3.Кислота
2.Основание 4.Щелочь и водород
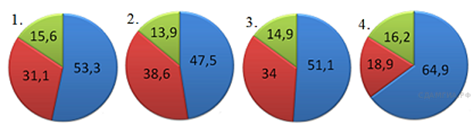
А 10. На какой диаграмме распределение массовых долей элементов соответствует количественному составу карбоната лития?
В1. Установите соответствие:
| Формула соединения | Название вещества |
| А. ZnO Б. Al (NO3)3 В.H2SO3 Г Ca(OH)2 | 1) Основание 2) Оксид 3) Кислота 4) Соль |
В 2. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры под которыми они указаны
В ряду химических элементов С---Si ----Ge
1.Увеличивается число электронных слоев
2.Уменьшается число протонов в ядре
3.Увеличивается значение электроотрицательности
4.усиливается металлические свойства
5.Увеличивается число электронов во внешнем слое
Часть С
С1. Используя метод электронного баланса, расставьте коэффициенты в уравнении, схема которой: KClO3 + P ----KCl + P2O5
Определите окислитель и восстановитель
C2.Какую массу воды нужно подвергнуть разложением электрическим током, чтобы получить 6,4 г. Кислорода
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|