
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
по теме: «Строение атома. Периодический закон и Периодическая система
Тест
по теме: «Строение атома. Периодический закон и Периодическая система
химических элементов Д.И. Менделеева»
| 1. | Чему равен заряд ядра атома (+Z), модель которого изображена на рисунке? 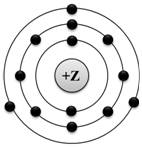 1) + 13
2) + 15
3) + 16
4) + 18
1) + 13
2) + 15
3) + 16
4) + 18
| ||||||||||||||||||||||
| 2. | Иону S2- соответствует электронная формула: 1) 1s2 2s22р63s23p6 2) 1s2 2s22p63s23p4 3) 1s2 2s2 2p6 4) 1s2 2s2 2p63s23p2 | ||||||||||||||||||||||
| 3. | Число энергетических слоев и число электронов во внешнем энергетическом слое атомов мышьяка равны соответственно: 1) 4, 6 2) 2, 5 3) 3, 7 4) 4, 5 | ||||||||||||||||||||||
| 4. | Установите соответствие между элементом и его электронной формулой:
| ||||||||||||||||||||||
| 5. | Внесите необходимые данные в пустые графы таблицы «Максимальное количество электронов на энергетическом подуровне»:
| ||||||||||||||||||||||
| 6. | Распределению электронов по энергетическим уровням в атоме элемента соответствует ряд чисел: 2, 8, 18, 6. В периодической системе этот элемент расположен в группе: 1) V A 2) VI A 3) V Б 4) VI Б | ||||||||||||||||||||||
| 7. | Химический элемент расположен в 3-м периоде III группе главной подгруппе. Характерным для него является образование: 1) водородного газообразного соединения состава Н2Э 2) высшего оксида состава ЭО3, кислотного характера 3) высшего оксида состава ЭО2, кислотного характера 4) высшего оксида состава Э2О3, амфотерного характера | ||||||||||||||||||||||
| 8. | Из приведенных химических элементов самый большой радиус атома имеет: 1) Bi 2) N 3) As 4) P | ||||||||||||||||||||||
| 9. | Химические элементы расположены в порядке возрастания их атомного радиуса в ряду: 1) Be, B, C, N 2) Rb, K, Na, Li 3) O, S, Se, Te 4) Mg, Al, Si, Р | ||||||||||||||||||||||
| 10. | Неметаллические свойства у элементов главных подгрупп усиливаются: 1) слева направо и сверху вниз 2) справа налево и сверху вниз 3) справа налево и снизу вверх 4) слева направо и снизу вверх | ||||||||||||||||||||||
| 11. | Химический элемент расположен в IV периоде, I А группе. Распределению электронов в атоме этого элемента соответствует ряд чисел: 1) 2, 8, 8, 2 2) 2, 8, 18, 1 3) 2, 8, 8, 1 4) 2, 8, 18, 2 | ||||||||||||||||||||||
| 12. | Изотопы одного и того же элемента отличаются друг от друга: 1) числом нейтронов 2) числом электронов 3) числом протонов 4) зарядом ядра | ||||||||||||||||||||||
| 13. | В ряду химических элементов Li → Be → B → C металлические свойства: 1) не изменяются 2) усиливаются 3) ослабевают 4) изменяются периодически | ||||||||||||||||||||||
| 14. | Из приведенных ниже металлов наиболее активным является: 1) бериллий 2) магний 3) кальций 4) барий | ||||||||||||||||||||||
| 15. | Число неспаренных электронов в атоме алюминия равно: 1) 3 2) 2 3) 1 4) 0 | ||||||||||||||||||||||
| 16. | Среди перечисленных элементов V группы типичным неметаллом является: 1) фосфор 2) мышьяк 3) сурьма 4) висмут | ||||||||||||||||||||||
| 17. | Химический элемент, формула высшего оксида которого R2O7, имеет электронную конфигурацию атома: 1) 1s22s22p63s1 2) 1s22s22p63s23p5 3) 1s22s22p63s23p64s1 4) 1s22s1 | ||||||||||||||||||||||
| 18. | У магния металлические свойства выражены: 1) слабее, чем у бериллия 2) сильнее, чем у кальция 3) сильнее, чем у алюминия 4) сильнее, чем у натрия | ||||||||||||||||||||||
| 19. | Установите соответствие между частицей и ее электронной конфигурацией:
| ||||||||||||||||||||||
| 20. | Одинаковое число протонов и нейтронов содержится в атоме: 1) железа-56 2) иода-127 3) кобальта-59 4) углерода-12 |
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|