
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Практическая работа по теме. Теоретические сведения
Практическая работа по теме
«Общие свойства металлов. Свойства оксидов и гидроксидов»
Цели: закрепить умения изображать реакции в молекулярном и ионном виде, характеризующие свойства металлов и их гидроксидов.
Теоретические сведения
Химические свойства металлов обуславливаются главным образом наличием в их атомах электронов, слабо связанных с ядром. Общим химическим свойством является способность металлов только отдавать электроны, превращаясь в положительно заряженные ионы по схеме:
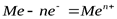 ,
,
где Ме – химический символ металла,
n – число электронов.
По степени легкости отдачи электронов в растворах металлы можно расположить в ряд напряжений металлов:
Li, Cs, K, Ca, Na, Mg, Al, Zn, Fe, Ni, Sn, Pb, H2, Cu, Ag, Hg, Au

усиление восстановительной способности
Гидроксиды металлов можно получить при действии щелочей на растворимые в воде соли металлов.
Гидроксиды железа, хрома и меди нерастворимы в воде, но растворимы в кислотах. Гидроксид хрома (III) растворим и в щелочах, то есть проявляет амфотерные свойства.
Пример. Получите гидроксид цинка, докажите его амфотерный характер. Запишите уравнения реакций в молекулярном и кратком ионном виде.
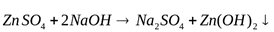
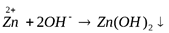
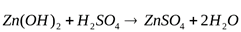
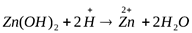
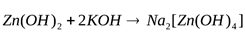
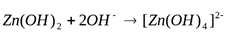
Вывод: гидроксид цинка является амфотерным соединением, так как вступает в реакцию с кислотой и щелочью.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|