
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Определение. К конспекту Ионная связьдля иформации (в конспект можно не писать)
Определение
Химическая связь, возникающая между ионами за счет электростатического притяжения, называется ионной связью.
Образуется между атомами металлов и неметаллов, т.е. между атомами, резко отличающимися друг от друга по значениям электроотрицательности. (Например, NaCl, K2O, LiF)
Механизм образования связи.
Атом неметалла забирает наружные электроны у атома металла и превращается в анион (отрицательно заряженный ион). Атом металла теряет электроны и превращается в катион (положительно заряженный ион). Ионы связаны электростатическими силами. Происходит полная отдача (принятие) валентных электронов, перекрывание облаков отсутствует, обобществления электронов не наблюдается.
Рассмотрим механизм образования молекулы фторида натрия: NaF
Электронная схема образования молекулы NaF:
| Na +11)2ē)8ē)1ē | Na0 – 1ē → Na+1 атом ион натрия натрия |
| F +9)2ē)7ē | F0 + 1ē → F-1 атом ион фтора фтора |
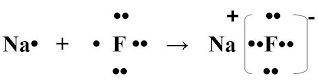
К конспекту "Ионная связь"для иформации (в конспект можно не писать)
Прежде, чем узнать, что такое ионная связь и как она образуется, побываем в одной удивительной стране.
Народ этой страны был беден, но беспечен. Хотя в карманах у большинства из них не было ни одной свободной монеты (а «валюта» в этой стране называлась электронами), никто не горевал по этому поводу. Напротив, если у них заводился хоть один лишний электрон, то характер их портился, они становились агрессивными и даже опасными, потому скорее хотели от него избавиться, чтобы стать опять добрыми и веселыми.
Надо сказать, что «высшая знать» этой страны отличалась от простых граждан своей скупостью. Свою «электронную валюту» они неохотно одалживали, и, наоборот, при малейшей возможности стремились забрать еще.
Давайте теперь разберёмся, кто же такие были «простые жители» (нежадные, положительные), а кем бала «знать» (жадные, отрицательные).
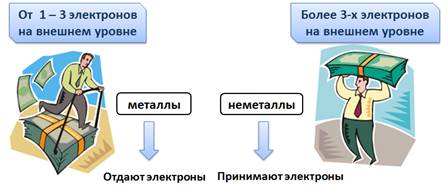
Речь в истории шла об элементах металлах и неметаллах. Разберёмся почему.
У атомов металлов на внешнем уровне всегда мало электронов (от одного до трех), естественно, что им легче отдать электроны для завершения энергетического уровня, а для неметаллов, у которых более трех электронов, легче присоединить электроны для завершения энергетического уровня.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|