
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Алгоритм начальной инфузионнои терапии гиповолемического шока
ГИПОВОЛЕМИЧЕСКИЙ ШОК
Среди различных типов шока чаще всего встречается гиповолемический шок (ГШ). Основу гемодинамических нарушений при этой форме шока составляют неадекватный ОЦК, уменьшение венозного возврата и снижение мое.
Гиповолемический шок характеризуется критическим уменьшением тканевой перфузии, вызванной острым дефицитом циркулирующей крови, уменьшением венозного притока к сердцу и вторичным снижением сердечного выброса. Основные причины, вызывающие снижение ОЦК: кровотечение, потеря плазматической жидкости и обезвоживание.
Среди причин ГШ роль плазмо- и кровопотери при травмах, операциях и ожогах в его развитии выявляется достаточно легко. Труднее диагностируются скрытые источники плазмо- и кровопотерь: кишечные кровотечения; скопление жидкости в брюшной полости и просвете кишечника при перитоните, кишечной непроходимости и панкреатите; секвестрации крови в местах переломов, травматических повреждений мягких тканей и т.д.
Патофизиологические изменения. Большая часть последовательных повреждений при ГШ связана со снижением эффективности перфузии, что ухудшает транспорт кислорода, питание тканей и приводит к тяжелым метаболическим нарушениям. В развитии ГШ выделяют следующие фазы:
• дефицит ОЦК;
• стимуляцию симпатико-адреналовой системы;
• шок.
I фаза— дефицит ОЦК. Острый дефицит объема крови приводит к уменьшению венозного притока к сердцу, снижению ЦВД и ДЗЛК. В результате этого снижается ударный объем сердца. В пределах 1 ч интерстициальная жидкость устремляется в капилляры, соответственно снижается объем интерстициального водного сектора. Это перемещение происходит в течение 36—40 ч от момента кровопотери. Общий объем транскапиллярного наполнения возрастает максимум на 1 л.
II фаза — стимуляция симпатико-адреналовой системы. Рефлекторная стимуляция барорецепторов вызывает активизацию симпатико-адреналовой системы. Возбуждение ее ведет к повышению секреции катехоламинов, содержание которых возрастает в десятки (норадреналин) и сотни (адреналин) раз. Увеличивается симпатический тонус сердца, вен и артериол, уменьшается вагусное влияние на сердце. Стимуляция бета-адренергических рецепторов приводит к увеличению сократительной способности миокарда и увеличению ЧСС. Стимуляция альфа-адренергических рецепторов вызывает сокращение селезенки, венозных сосудов, вазоконстрикцию в коже, скелетных мышцах, почках, приводя к повышению ОПСС и централизации кровообращения. Этот механизм направлен на поддержание МОС, АД, ЦВД, кровообращения в мозге и сердце за счет ухудшения кровообращения в органах, иннервируемых блуждающим нервом (печень, поджелудочная железа, кишечник), а также в почках, коже и мышечной системе. Вазоконстрикция объемных сосудов, вызывающая уменьшение емкости венозных сосудов, ведет к диспропорции между объемом крови и емкостью сосудистого русла. В коротком интервале времени эта реакция является защитной и при быстрой нормализации объема крови наступает выздоровление. Если же дефицит ОЦК сохраняется, то на первый план выступают отрицательные последствия длительной ишемии, за счет которых достигается централизация кровообращения.
Активация ренин—ангиотензин—альдостероновой системы вызывает задержку натрия, содержащегося преимущественно в интерстициальном водном секторе. Этот механизм способствует задержке жидкости и восполнению объема этого сектора.
III фаза — гиповолемический шок. Дефицит объема крови, уменьшение венозного возврата и давления наполнения сердца, МОС, АД и тканевой перфузии на фоне продолжающейся адренергической реакции являются основными звеньями ГШ.
Гемодинамика. В результате симпатоадренергической реакции происходит сужение сосудов, особенно артерий. Депо крови опустошаются, сила и ЧСС повышаются, происходит мобилизация крови из легких, открываются артериовенозные шунты. Объем внутрисосудистого водного сектора частично увеличивается вследствие притока интерстициальной жидкости. Благодаря этому на первом этапе ГШ может наблюдаться гипердинамическая реакция кровообращения, обусловленная снижением доставки кислорода к тканям. Начинающийся шок, характеризующийся нормальным АД, тахикардией и холодными кожными покровами, называют фазой I, или компенсированным шоком [Хартиг В., 1982].
При продолжающемся кровотечении снижается не только УО, но и МОС. Одновременно со снижением СВ возрастает ОПСС. Вазоконстрикция пре- и посткапиллярных сосудов приводит к снижению капиллярного кровотока. С прогрессированием шока накопление кислых продуктов метаболизма сопровождается расширением прекапиллярных сфинктеров, в то время как посткапиллярные сфинктеры остаются суженными (большая часть крови депонируется в капиллярах). Феномен централизации кровообращения сопровождается полиорганной недостаточностью.
Снижение кровотока, ведущее к ишемии органов и тканей, происходит в определенной последовательности: кожа, скелетные мышцы, конечности, почки, органы брюшной полости, легкие, сердце, мозг.
При продолжающейся кровопотере АД становится ниже 100 мм рт.ст., а пульс 100 или более в минуту. Отношение ЧСС/АДсист. — индекс шока (ИШ) — выше 1. Это состояние (холодная кожа, гипотензия, тахикардия) определяется как фаза II, или декомпенсированный шок (табл. 16.1).
Таблица 16.1.
Гемодинамика при гиповолемическом шоке

Реологические нарушения. Секвестрация крови и замедление капиллярного кровотока приводят к спонтанному свертыванию крови в капиллярах. Типичными клеточными агрегантами являются скопления эритроцитов и тромбоцитов. Стаз крови и выход из поврежденных клеток субстанций, активирующих свертывание, способствуют возникновению коагулопатии потребления, т.е. расходу определенных компонентов свертывания: тромбоцитов, фибриногена, протромбина и ДВС.
Транспорт кислорода. При ГШ стимулируется анаэробный метаболизм, который в свою очередь обусловливает ацидоз. Дефицит глобулярного объема (ГО) сопровождается соответственным снижением СаО2. При относительно умеренной кровопотере DO2 поддерживается гипердинамическим режимом кровообращения. Снижение СВ при значительной кровопотере и шоке ведет к резкому уменьшению DО2.
Динамика доставки кислорода к тканям. В табл. 16.2 представлены данные об изменениях DО2 в зависимости от степени кровопотери и компенсаторной реакции кровообращения. При кровопотере до 10 % ОЦК и 30 % глобулярного объема сердечный индекс (СИ) колеблется в нормальных пределах и DО2 не нарушена. При кровопотере до 25 % и дефиците глобулярного объема до 40 % СИ возрастает до 5,3 л/(мин-м2), работа левого желудочка увеличивается до 13,2 кг/мин, благодаря чему DО2 фактически не нарушается. Снижение DО2 до 400—475 мл/(мин-м2) наступает при более значительной кровопотере — более 30 % ОЦК и дефиците глобулярного объема более 50 %. При шоке наблюдается гиподинамический режим кровообращения, СИ и РЛЖ снижены до критического уровня. Индекс доставки кислорода снижен до 230—137 мл/мин/м2, т.е. в 3—4 раза по сравнению с нормой (520—720 мл/мин/м2).
Таблица 16.2.
Доставка кислорода к тканям в зависимости от степени кровопотери и гемодинамической компенсации
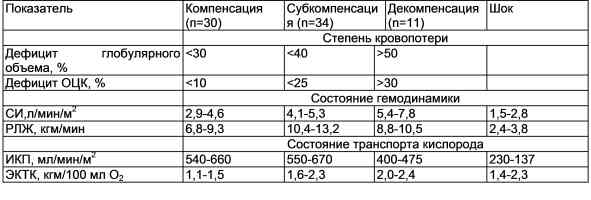
Примечание. ИКП — индекс кислородного потока; ЭКТК — энергокоэффициент транспорта кислорода.
VO2 тканей не соответствует их потребностям для аэробного метаболизма. Потребление кислорода, сниженное во время шока, закономерно возрастает при успешном лечении в постшоковом периоде. При этом сверхнормальные значения VО2 отражают нормальную физиологическую реакцию, направленную на ликвидацию кислородной задолженности тканям [Марино П., 1998].
Транспорт кислорода при гиповолемическом шоке:
• SaO2 и РаO2 снижены в результате нарушений вентиляционно-перфузионных соотношений в легких;
• СаО2 снижено в результате уменьшения глобулярного объема, уменьшения SaO2 и РаО2;
• DO2 снижается с момента перехода гипердинамического состояния кровообращения в нормо- или гиподинамический тип:
• VO2, как правило, снижено;
• уровень лактата крови повышен.
Полиорганная недостаточность. Длительная ишемия ренальной и чревной областей сопровождается недостаточностью функций почек и кишечника. Мочевыделительная и концентрационная функции почек снижаются, но при своевременном лечении это состояние может быть обратимым. При длительной ишемии почки полностью теряют свои гомеостатические функции.
При длительной ишемии развиваются некрозы в слизистой оболочке кишечника, печени, почках и поджелудочной железе. Нарушается барьерная функция кишечника. Бактериальные токсины, гистамин и метаболиты поступают в кровоток. Эти вещества могут активизировать кининовую систему и угнетать функцию миокарда. Процесс в легких развивается по типу РДСВ. Снижение мозгового кровотока сопровождается нарушениями функций ЦНС вплоть до комы.
Полиорганная недостаточность при ГШ:
• почки — олигурия -> анурия;
• кишечник — паралитический илеус, образование острых язв, нарушение барьерной функции, выход токсинов в кровь;
• печень — некрозы, снижение функции;
• сердце — нарушение механизма Франка—Старлинга, снижение сократительной способности миокарда;
• легкие — нарушения вентиляционно-перфузионных отношений, развитие РДСВ;
• мозг — затемнение сознания, кома.
Клинические критерии шока:
• частый малый пульс;
• снижение систолического АД;
• снижение ЦВД;
• холодная, влажная, бледно-цианотичная или мраморная кожа;
• замедленный кровоток в ногтевом ложе;
• температурный градиент более 3 °С;
• олигурия.
Эти симптомы соответствуют декомпенсации кровообращения и являются показанием к немедленной противошоковой терапии. АД может удерживаться достаточно долго на нормальных цифрах, например при медленном снижении ОЦК. Вазоконстрикция кожных покровов обычно протекает без видимого цианоза.
СВ сам по себе не может быть показателем адекватности перфузии тканей. Выраженная вазоконстрикция нарушает распределение кровотока: большая часть органов и тканей страдает от дефицита перфузии при относительно нормальной работе сердца как насоса. Достаточно точный показатель кровообращения — определение фактического МОС на этапах интенсивной терапии.
ЦВД может быть повышенным при сердечной недостаточности и ИВЛ, особенно в режиме ПДКВ. Это ни в коей мере не умаляет важности определения ЦВД как важнейшего критерия ГШ.
Сложность патогенеза исключает существование какого-то одного показателя, отражающего всю гамму изменений при шоке, например в кригериях транспорта кислорода. На суммарной оценке транспорта кислорода сказываются: собственно перфузия тканей, зависящая от системы кровообращения, и состояние окислительного метаболизма, т.е. то конечное звено, которое определяет тяжесть последствий неадекватной тканевой перфузии.
Клиническая картина в большей степени зависит от объема потерянной крови, скорости кровопотери и компенсаторных механизмов организма. Имеют значение и другие факторы: возраст, конституция, сопутствующие заболевания сердца, легких.
Важнейшие критерии шока: частота пульса, АД, индекс Аллговера, ЦВД, клинические симптомы нарушений гемодинамики и функций органов.
Для определения зависимости шока от кровопотери удобно пользоваться 4-степенной классификацией (американская коллегия хирургов):

Потеря 15 % ОЦК или менее. Клинические признаки кровопотери могут отсутствовать. У больного, находящегося в горизонтальном положении, нет симптомов кровопотери. Единственным признаком может быть увеличение частоты пульса не менее чем на 20 в минуту, возникающее при вставании с постели.
Потеря от 20 до 25 % ОЦК. Основной симптом — ортостатическая гипотензия — снижение систолического АД не менее чем на 15 мм рт.ст. В положении лежа АД обычно сохранено, но может быть несколько снижено [Марино П., 1998]. Это состояние при продолжающемся кровотечении может быстро перейти в следующую фазу. Систолическое давление превышает 100 мм рт.ст., частота пульса 100—110 уд/мин, индекс шока не более 1 [Хартиг В., 1982].
Потеря от 30 до 40 % ОЦК. Клиническая картина соответствует умеренному или компенсированному шоку: холодные кожные покровы, симптом «бледного пятна», частота пульса более 100 в минуту, артериальная гипотензия в положении лежа на спине, олигурия. Критическими являются падение систолического АД ниже 100 мм рт.ст. и учащение пульса более 100 в минуту. Увеличение индекса шока больше 1.
Потеря более 40 % ОЦК. Клиническая картина соответствует тяжелому или декомпенсированному шоку: холодные кожные покровы, резкая бледность, мраморность кожи, нарушение сознания вплоть до комы, отсутствие пульса на периферических артериях, падение АД, СВ. Индекс шока более 1,5. Анурия.
Потеря более 40 % ОЦК потенциально опасна для жизни.
Лечение. Главнейшее звено, которое должно восстанавливаться при ГШ в первую очередь, — транспорт кислорода. Этот показатель ГТТТ зависит от:
• недостаточного венозного притока к сердцу, связанного с ним низкого СВ и гиподинамического состояния кровообращения;
• низкого содержания кислорода в артериальной крови в связи с потерей гемоглобина.
Важную роль играет дефицит интерстициальной жидкости, нарушающий транскапиллярный обмен жидкости и кислорода.
Программа интенсивного лечения ГШ:
• быстрое восстановление внутрисосудистого объема;
• улучшение функции сердечно-сосудистой системы;
• восстановление объема циркулирующих эритроцитов;
• коррекция жидкостных дефицитов;
• коррекция нарушенных систем гомеостаза.
Из всех имеющихся в настоящее время средств для быстрого восстановления внутрисосудистого объема жидкости наиболее эффективными являются гетерогенные коллоидные растворы: декстран и крахмал, оказывающие выраженное гемодинамическое противошоковое действие. Коллоидные растворы по сравнению с кристаллоидными значительно быстрее восстанавливают ОЦП и, таким образом, обеспечивают достаточный приток крови к сердцу. Доказано, что СВ повышается быстрее в тех случаях, когда первично проводится инфузия коллоидных растворов, обладающих объемозамещающим и реологическим свойствами. По сравнению с цельной кровью и эритроцитной массой в первичном возмещении их объема эти препараты имеют несомненное преимущество [Марино П., 1998].
Даже при сниженном содержании кислорода в артериальной крови возросший СВ может обеспечить адекватную DO2 к тканям.
При первичном возмещении коллоидные растворы комбинируют с электролитными инфузионными растворами, содержащими Na+ и СГ. Электролитные растворы (раствор Рингера, 0,9 % раствор натрия хлорида) необходимы для коррекции интерстициального объема. Скорость инфузии плазмозамещающих и электролитных растворов определяется состоянием больного. При тяжелом шоке проводят струйное введение растворов.
Показания к гемотрансфузии должны быть очень строгими. Это особенно важно в свете последних данных об иммунодепрессивных состояниях. Несмотря на все имеющиеся ограничения к гемотрансфузии, показанием к ее назначению служит значительное уменьшение уровня гемоглобина. Ориентировочно этот уровень может быть равен 80 г/л, но до недавнего времени показанием к гемотрансфузии считалось снижение уровня гемоглобина крови ниже 100 г/л. Не оспаривая в целом эти положения, заметим, что наиболее достоверным обоснованием тактики является уровень транспорта кислорода и особенно его потребление тканями. Полагаем, что старое правило — чем больше кровопотеря, тем больше показаний к гемотрансфузии — пока еще остается в силе. При кровопотере, равной 50 % ОЦК, несомненно, требуется обязательное возмещение части этой кровопотери препаратами крови — эритроцитной массой или цельной кровью. При этом не следует ограничиваться гетерогенными плазмозамещающими растворами, а использовать плазму или растворы альбумина.
Критерии инфузионной терапии
• восстановление адекватного СВ:
СИ — 2,5—3,5 л/мин/м2 или выше;
АДсист — не ниже 100 мм рт.ст.;
ЧСС — 100 уд/мин или менее;
ДНЛЖ — 12—16 мм рт.ст.;
ОПСС - 1200-2500 дин/с.см^м2.
При продолжающейся сердечной недостаточности, не связанной с дефицитом сосудистого объема, показано назначение симпатомиметических средств — добутамина или допамина. Наиболее приемлемый метод оценки показателей центральной гемодинамики — бескровный динамический контроль (мониторинг, аппарат «РЕО-ДИН»);
• динамический контроль (мониторинг жидкостного распределения в водных секторах: сосудистом, интерстициальном и клеточном) осуществляется путем бескровного метода по принципу Томассета. Работа монитора трансфузиолога основана на принципе импедансометрии зондирующими токами определенной частоты. Сопротивление тканей измеряется в зависимости от их наполнения жидкостью. Этот метод позволяет определять объемы общей, вне- и внутриклеточной, интерстициальной и сосудистой жидкости в сравнении с должной величиной и представить в виде таблицы, тренда или диаграммы [Малышев В.Д. и др., 1998];
• почасовой диурез должен составлять 40—50 мл/ч. На фоне достаточного жидкостного восполнения для стимуляции диуреза могут быть использованы фуросемид (20—40 мг и более) или допамин в малых дозах (3—5 мкг/кг/мин), улучшающий ренальное кровообращение и способствующий профилактике почечной недостаточности;
• динамический контроль газов крови и КОС. Эти показатели необходимы для расчетов транспорта кислорода на всех этапах лечения. В норме индекс DО2 равен 520—720 мл/мин/м2. Для измерения потребления кислорода тканями необходимо знать содержание кислорода не только в артериальной, но и в смешанной венозной крови (CvO2). Увеличение дефицита оснований может указывать на избыток молочной кислоты, являющейся показателем анаэробного обмена;
• прочие показатели гомеостаза. Важно поддерживать коллоидно-осмотическое давление плазмы крови на уровне 20—25 мм рт.ст., осмолярность плазмы в диапазоне 280—300 мосм/л, уровень альбуминов и общего белка 37—50 г/л, глюкозы 4—5 ммоль/л, степень гемодилюции 27—35 %; контролировать состояние свертывающей и противосвертывающей систем крови.
Первичное возмещение кровопотери (схема 16.1). Необходимые расчеты у взрослого мужчины ОЦК определяют по формуле: 70 х масса тела (кг). У женщин: 65 х масса тела. Таким образом, у мужчины с массой тела 70 кг ОЦК будет равен:
70х70 = 4900 мл (5000 мл);
20 % ОЦК = (500х20) : 100 = 1000 мл;
30 % ОЦК = (5000х30) : 100 = 1500 мл;
50 % ОЦК - (5000х50) : 100 = 2500 мл.
У тучных и пожилых людей ОЦК примерно на 5 мл/кг ниже указанных величин. ОЦК у лиц атлетического телосложения примерно на 5 мл/кг выше средней нормы. В схеме 16.1 приведены алгоритмы возмещения кровопотери.
Схема 16.1.
Алгоритмы первичного возмещения кровопотери
(мужчина средних лет, масса тела 70 кг, кровопотеря 20,30 и 50 % ОЦК)

При массивной кровопотере, превышающей 50 % ОЦК, препаратами выбора являются человеческий альбумин и эритроцитная масса. Удельный вес синтетических коллоидов при этом из-за риска аллергических реакций должен быть уменьшен. Кровопотеря, превышающая ОЦК, сопровождается значительным снижением содержания тромбоцитов и факторов свертывания. В связи с этим при массивной кровопотере необходимо использовать свежую тромбоцитную массу и свежезамороженную плазму. Коррекция же системы гемостаза должна проводиться в зависимости от изменений коагулограммы.
Окончательное возмещение кровопотери требует точного контроля ее объема и секторального распределения. На этом этапе важно определение как количественных, так и качественных критериев инфузионной терапии! При продолжающемся дефиците ОЦП показаны инфузии плазмы, протеина и альбумина (необходимы контроль ОЦП и КОД плазмы, концентрации общего белка и альбумина).
Окончательное возмещение кровопотери. Под окончательным возмещением кровопотери подразумевается полная коррекция всех нарушений — систем гомеостаза, секторального распределения жидкости, осмолярности, концентрации гемоглобина и белков плазмы. При продолжающемся дефиците ОЦП проводят инфузии коллоидных, преимущественно аутогенных растворов: плазмы, протеина и альбумина.
Критерии возмещения кровопотери: объем внутрисосудистой жидкости (плазмы) — 42 мл/кг массы тела, концентрация общего белка — не ниже 60 г/л, уровень альбуминов плазмы — не ниже 37 г/л, КОД плазмы — не ниже 20 мм рт.ст.
При дефиците объема циркулирующих эритроцитов, превышающем 30 %, проводят инфузии эритроцитной массы. Концентрация гемоглобина в плазме не должна быть ниже 80 г/л (при условии адекватной доставки и потребления кислорода тканями). В противном случае поддерживают концентрацию гемоглобина на уровне 100 г/л.
При дефиците интерстициальной жидкости требуется дополнительное введение изотонических растворов, содержащих натрий и хлор. При возмещении кровопотери следует учитывать потерю жидкости, связанную с перспирацией и возможной торакоабдоминальной операцией. Если кровопотеря связана с травмой или обширной операцией, общий дефицит жидкостного объема может значительно превышать приведенные расчеты, а характер водно-электролитных нарушений может быть иным. Поступление воды и натрия в клетки способствует развитию отека. Из клеток же во внеклеточное пространство перемещаются калий и фосфаты — механизм, описанный при тяжелой травме и стрессе — «трансминерализация».
При избытке интерстициальной жидкости требуется прекращение инфузии кристаллоидных растворов. При значительном превышении объема интерстициального пространства показаны диуретики. Критерии адекватного возмещения интерстициального сектора (объем его составляет в среднем 15 % массы тела и легко определяется аппаратом «спутник трансфузиолога»): осмолярность внеклеточной жидкости 280—300 мосм/л, концентрация натрия 130—150 ммоль/л, диурез 50 мл/ч.
Дефицит жидкости во внутриклеточном водном пространстве (клеточная дегидратация) может возникать при гиперосмолярном состоянии плазмы, например при избытке ионов Na+ Сl-, недостаточном их возмещении безэлектролитными растворами. Коррекция — восстановление осмолярности плазмы, инфузии растворов глюкозы с инсулином.
Избыток внутриклеточной жидкости может наблюдаться при неустраненной гипонатриемии, сниженной осмолярности плазмы, инфузиях безэлектролитных соединений. При дисбалансе K+, Mg2+ Ca2+ нарушениях КОС также необходима коррекция.
Новые подходы к лечению гиповолемического шока. Травма в сочетании с ГШ является ведущей причиной смертности людей молодого возраста. Одним из факторов отсроченной смерти является развитие синдрома полиорганной недостаточности (СПОН) в постреанимационном периоде. Первичными факторами, которые определяют риск развития СПОН вследствие травмы и кровопотери, считают нарушения микроциркуляции, вызывающие тканевую гипоксию и расстройства клеточных функций. Причинами снижения кровотока в тканях и органах служат гиповолемия и низкое перфузионное давление.
В настоящее время выделяют следующие механизмы, вызывающие СПОН:
• высвобождение различных медиаторов, особенно цитокинов (интерлейкины, интерферон, туморнекротизирующий фактор и др.), активацию макрофагов;
• нарушение микроциркуляции и повреждение эндотелия сосудов;
• снижение барьерной функции кишечника, что ведет к проникновению через поврежденную стенку кишки бактерий или эндотоксинов.
Первичная инфузия при тяжелом кровотечении обычно заключается в быстром вливании коллоидных и кристаллоидных растворов. Однако в тяжелых случаях нагрузка объемом вводимой жидкости не может восстановить трофический потенциал кровотока и клеточный гомеостаз, особенно в паренхиматозных органах, и предотвратить трансформацию шока в СПОН. При введении большого количества жидкости имеется риск развития тяжелого отека слизистой оболочки кишечника, легких, клеточных структур и нарушений микроциркуляции.
Использование гипертонического раствора натрия хлорида при ГШ, как в эксперименте, так и в клинике, показало его несомненные преимущества. Доказана способность 7,5 % солевого раствора повышать системное АД, СВ, улучшать микроциркуляцию и выживаемость. Новизна предлагаемой концепции состоит в действии на микроциркуляцию и получении немедленного улучшения центральной гемодинамики при объеме первичной инфузии из расчета 4 мл/кг массы тела у больных с гиповолемией и шоком. Внутривенная инфузия небольшого объема 7,5 % раствора натрия хлорида приводит к недолговременному, но существенному повышению осмолярности плазмы (7,5 % раствор натрия хлорида имеет осмолярность 2400 мосм/л).
Одновременно применяют гетерогенные коллоидные растворы (10 % раствор декстрана-60-70, реже гидрооксиэтилкрахмал), которые повышают онкотическое давление плазмы и тем самым оказывают гемодинамическое действие. Одновременное применение гипертонического раствора натрия хлорида и коллоидов проявляется в сочетанном эффекте, связанном с повышением осмолярности плазмы и онкотического давления. Цель применения коллоидов в этом сочетании — удержание возмещенного внутрисосудистого объема в течение длительного времени.
Основные эффекты, наблюдаемые при введении гипертонического раствора натрия хлорида при ГШ:
• быстро повышает АД и СВ;
• увеличивает преднагрузку и снижает ОПСС;
• повышает эффективную тканевую перфузию;
• снижает риск отсроченной полиорганной недостаточности.
В то же время не следует забывать об опасностях применения солевых растворов. К потенциальным опасностям их использования следует отнести развитие гиперосмолярного состояния, отрицательный инотропный эффект (вследствие быстрой инфузии), усиление кровопотери в случае неостановленного кровотечения.
Главным отличием данного метода является «малообъемный принцип», т.е. общий объем жидкостного возмещения кровопотери должен быть во много раз меньше, чем при использовании изотонических кристаллоидных растворов.
Методика применения 7,5 % раствора натрия хлорида при ГШ:
• общий объем вводимого гипертонического раствора хлорида натрия должен составлять 4 мл/кг массы тела, т.е. от 100 до 400 мл;
• раствор вводят дробно болюсно по 50 мл с небольшими перерывами (10-20 мин);
• введение солевого раствора комбинируют с 10 % раствором декстрана-60-70;
• введение растворов прекращают при стабильном АД, стабильной гемодинамике и других признаках отсутствия шока.
Гемодинамический мониторинг по технологии «МЕДАСС». Мониторы параметров центральной гемодинамики (РПЦ-01, РПКА 2-01) с математическими программами обработки реосигнала «Импекард-3», «Реодин», «Реодин-орто» предназначены для бескровного динамического исследования всех важнейших показателей: ЧСС, ударного и минутного объемов сердца, СИ, индекса ударной и минутной работы левого желудочка, ДНЛЖ, ОПСС и др.
РПЦ-01, РПКА 2-01 прошли технические и клинические испытания и рекомендованы Министерством здравоохранения РФ к применению в клинической практике. Область применения очень широкая — от функциональной диагностики до мониторного контроля в интенсивной терапии.
Комплекс содержит измерительный реографический преобразователь IBM-совместимую персональную ЭВМ и программное обеспечение. В выходных документах (данные) имеются таблица основных параметров центральной гемодинамики, обозначен тип кровообращения (синтезированное заключение, основанное на анализе сочетания основных параметров гемодинамики), кривая Франка—Старлинга, временные тренды и графики перечисленных параметров. Количество исследований у пациента не ограничено.
Гидродинамический мониторинг по технологии «МЕДАСС». Анализатор оценки баланса водных секторов организма «АВС-01 МЕДАСС» предназначен для оценки и мониторирования баланса водных сред организма. Область применения анализатора — реаниматология и интенсивная терапия, анестезиология, терапия и др.
Принцип работы анализатора основан на использовании зависимости баланса вне- и внутриклеточной жидкости от соотношения электрического сопротивления тканей организма на высокой и низкой частоте. Электродная система анализатора подключается к голеням и запястьям. Обработка и представление полученных результатов осуществляются персональной ЭВМ, на экране которой и, по желанию врача, на бумажном носителе могут быть отражены содержание и тренды вне- и внутриклеточной жидкости в тканях, ОЦК в абсолютных значениях, их соотношение с должными величинами и другие параметры водно-солевого баланса.
Таблица данных экспресс-исследования содержит величину безжировой массы, измеренные и должные величины общего объема воды, объема внеклеточной и внутриклеточной воды, ОЦК и ОЦП. На основании полученных результатов врач определяет дальнейшую программу лечения. Динамическое исследование водных секторов — это контроль адекватности проводимой жидкостной терапии.
Алгоритм начальной инфузионнои терапии гиповолемического шока
(у пациентов с тяжёлой степенью дегидратации и клиникой шока I ЭТАП программы ИТ может начинаться с этого алгоритма). Кроме этого, данный подход может использоваться у других групп больных которым требуется быстрое увеличение преднагрузки.

Показатели адекватности перфузии
1. Уровень сознания (у больных с черепно-мозговой травмой этот критерий утрачивает свою ценность).
2. Перфузия конечностей - скорость капиллярного наполнения при нажатии на ногтевое ложе (в норме < 2 - 3 секунд), цвет и температура кожи.
3. Частота сердечных сокращений.
4. Кровяное давление, тоны сердца.
5. Диурез - норма у детей не менее 0,8 - 1 мл/кг/час, у новорождённых — не менее 0,5 - 0,6 мг/кг/час.
6. рН - метаболический ацидоз, повышение уровня лактата указывает на неадекватную перфузию.
Состав внеклеточной жидкости и растворов для инфузионной терапии (ммоль/л)
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|