
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Описание метода измерений
Работа № 15
Изучение вязкости воздуха
Цель: определение коэффициента вязкости воздуха и исследование зависимости объёма воздуха, протекающего через капилляр, от его размеров.
Оборудование: набор капилляров, стеклянный баллон, насос, манометр, барометр, секундомер.
Описание метода измерений
Явления переноса – это процессы установления равновесия в системе путём переноса массы (диффузия), энергии (теплопроводность) и импульса молекул (внутреннее трение или динамическая вязкость).
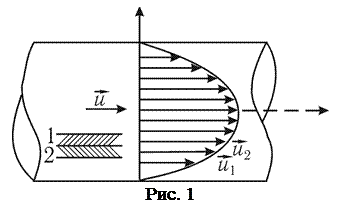 В явлении вязкости наблюдается перенос импульса от более быстрых участков потока к менее быстрым. При течении газа или жидкости, например внутри трубы, скорости слоев различны: их распределение при ламинарном течении показано на рис. 1 (длина стрелки показывает скорость данного слоя). Причиной этого является хаотическое тепловое движение молекул, при котором они непрерывно переходят из слоя в слой и в соударениях с другими молекулами обмениваются импульсами. Так, молекулы второго слоя, попадая в слой 1, переносят свой импульс направленного движения
В явлении вязкости наблюдается перенос импульса от более быстрых участков потока к менее быстрым. При течении газа или жидкости, например внутри трубы, скорости слоев различны: их распределение при ламинарном течении показано на рис. 1 (длина стрелки показывает скорость данного слоя). Причиной этого является хаотическое тепловое движение молекул, при котором они непрерывно переходят из слоя в слой и в соударениях с другими молекулами обмениваются импульсами. Так, молекулы второго слоя, попадая в слой 1, переносят свой импульс направленного движения  , а в слой 2 приходят молекулы с меньшим импульсом
, а в слой 2 приходят молекулы с меньшим импульсом  . В результате второй слой тормозится, а первый – ускоряется. Опыт показывает, что импульс dp, передаваемый от слоя к слою через поверхность S, пропорционален градиенту скорости du/dx, площади S и времени переноса dt:
. В результате второй слой тормозится, а первый – ускоряется. Опыт показывает, что импульс dp, передаваемый от слоя к слою через поверхность S, пропорционален градиенту скорости du/dx, площади S и времени переноса dt:
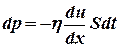 .
.
В результате между слоями возникает сила внутреннего трения (закон Ньютона)
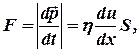 (1)
(1)
где h – коэффициент вязкости среды.
Для идеального газа коэффициент вязкости
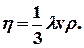 (2)
(2)
Средняя длина свободного пробега молекул
 , (3)
, (3)
где k= 1,38×10–23 Дж/К – постоянная Больцмана,
d – эффективный диаметр молекул (для воздуха d@ 4×10–10 м),
Т, Р – температура и давление газа.
Средняя скорость теплового движения молекул
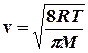 , (4)
, (4)
где R= 8,31 Дж/моль×К – универсальная газовая постоянная,
М – масса одного моля газа (для воздуха М = 28,9 г/моль).
Плотность газа согласно уравнению состояния идеального газа
 . (5)
. (5)
При ламинарном течении через трубу круглого сечения радиусом r (капилляр) и длиной L за время t протекает газ или жидкость, объём Vкоторых определяется по формуле Пуазейля:
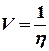
 , (6)
, (6)
где DР – разность давлений на концах капилляра.
Если в баллоне создать избыточное над атмосферным Р0 давление
DР= Р – Р0 = rжgh (rж – плотность жидкости в манометре, h – разность уровней жидкости) и соединить капилляр с атмосферой, то за время dt через капилляр вытечет некоторое количество воздуха, масса которого
dm= rdV, (7)
где r – плотность воздуха в капилляре, зависящая (см. формулу (5)) от давления воздуха, dV – объём вышедшего воздуха.
Давление воздуха в капилляре изменяется от Р0 до Р0 + rgh, но так, как
rgh<< Р0, то с достаточной точностью можно принять давление воздуха в капилляре равным атмосферному Р0. Тогда плотность воздуха (из уравнения Менделеева–Клапейрона)
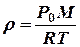 . (8)
. (8)
Объём воздуха dV, прошедшего через капилляр за время dt, описывается формулой Пуазейля (6):
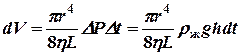 , (9)
, (9)
а масса воздуха, вытекающего из баллона, с учётом формул (8) и (9)
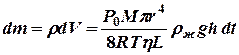 . (10)
. (10)
Из уравнения состояния идеального газа выразим изменение массы газа dm в баллоне через уменьшение давления в нём.
Так как dP= rжgdh, то
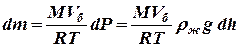 . (11)
. (11)
Исключая dmиз уравнений (10) и (11), получаем
 . (12)
. (12)
Решая это дифференциальное уравнение при условии, что за время опыта давление в баллоне уменьшится от rжgh0 до rжgh, получаем
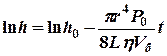 . (13)*
. (13)*
Таким образом, формула (13) связывает разность давлений h на концах капилляра с временем t истечения воздуха, его вязкостью h и размерами капилляра r и L.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|