
- Автоматизация
- Антропология
- Археология
- Архитектура
- Биология
- Ботаника
- Бухгалтерия
- Военная наука
- Генетика
- География
- Геология
- Демография
- Деревообработка
- Журналистика
- Зоология
- Изобретательство
- Информатика
- Искусство
- История
- Кинематография
- Компьютеризация
- Косметика
- Кулинария
- Культура
- Лексикология
- Лингвистика
- Литература
- Логика
- Маркетинг
- Математика
- Материаловедение
- Медицина
- Менеджмент
- Металлургия
- Метрология
- Механика
- Музыка
- Науковедение
- Образование
- Охрана Труда
- Педагогика
- Полиграфия
- Политология
- Право
- Предпринимательство
- Приборостроение
- Программирование
- Производство
- Промышленность
- Психология
- Радиосвязь
- Религия
- Риторика
- Социология
- Спорт
- Стандартизация
- Статистика
- Строительство
- Технологии
- Торговля
- Транспорт
- Фармакология
- Физика
- Физиология
- Философия
- Финансы
- Химия
- Хозяйство
- Черчение
- Экология
- Экономика
- Электроника
- Электротехника
- Энергетика
Комментарии 5 страница
7) Трёхгрупповая метафаза и метафаза с полярными хромосомами характеризуется наличием в метафазе помимо основной экваториальной пластинки ещё двух групп или отдельных («полярных») хромосом в области полюсов деления клетки[105]. Хромосомы сохраняются вблизи полюсов веретена из-за отставания в процессе метакинеза, а не из-за преждевременного расхождения. Причинами отставания могут служить повреждения кинетохора или дезорганизация отдельных хромосомальных нитей, участвующих в движении отстающих хромосом[106].
8) Полая метафаза представляет собой кольцевое скопление хромосом в экваториальной пластинке вдоль периферии клетки[107].
III. Патология митоза, связанная с нарушением цитотомии[править | править код]
Различают две группы патологий митоза, связанные с нарушением цитотомии: раннюю цитотомию, берущую начало ещё в анафазе; либо наоборот, запаздывание или полное отсутствие цитотомии, в результате чего формируются двуядерные клетки, либо образуется одно полиплоидное ядро[107].
Типы митоза[править | править код]
Выработка единой типологии и классификации митозов осложняется целым спектром признаков[~ 9], которые в различных комбинациях создают разнообразие и неоднородность картин митотического деления. При этом отдельные варианты классификации, разработанные применительно к одним таксонам, являются неприемлемыми в отношении других, поскольку не учитывают специфики их митозов. Например, отдельные варианты классификации митозов, свойственных животным или растительным организмам, оказываются неприемлемыми для водорослей[108].
Одним из ключевых признаков, лежащих в основе различных типологий и классификаций митотического деления, является поведение ядерной оболочки. Если образование веретена и само митотическое деление протекает внутри ядра без разрушения ядерной оболочки, то такой тип митоза называют закрытым. Митоз с распадом ядерной оболочки, соответственно, называется открытым, а митоз с распадом оболочки только на полюсах веретена, с образованием «полярных окон» — полузакрытым[108][109].
Ещё одним характерным признаком является тип симметрии митотического веретена. При плевромитозе веретено деления билатерально симметрично либо асимметрично и состоит, как правило, из двух полуверетён, располагающихся в метафазе-анафазе под углом друг к другу. Для категории ортомитозов характерна биполярная симметрия веретена деления, а в метафазе зачастую наблюдается различимая экваториальная пластинка[109].
В рамках обозначенных признаков наиболее многочисленным является типичный открытый ортомитоз. Данный тип митоза характерен для животных, высших растений и некоторых простейших[110].
Варианты классификации митозов[править | править код]
| 7 типов митоза простейших[109]: · Закрытый внутриядерный плевромитоз · Закрытый внутриядерный ортомитоз · Закрытый эвгленоидный митоз · Закрытый внеядерный плевромитоз · Полузакрытый плевромитоз · Полузакрытый ортомитоз · Открытый ортомитоз (эумитоз) | 6 типов митоза водорослей[108]: · Закрытый центрический · Закрытый ацентрический · Полузакрытый центрический · Полузакрытый ацентрический · Открытый центрический · Открытый ацентрический |  Основные типы митоза у водорослей: 1. закрытый центрический, 2. закрытый ацентрический, 3. полузакрытый центрический, 4. полузакрытый ацентрический, 5. открытый центрический, 6. открытый ацентрический
Основные типы митоза у водорослей: 1. закрытый центрический, 2. закрытый ацентрический, 3. полузакрытый центрический, 4. полузакрытый ацентрический, 5. открытый центрический, 6. открытый ацентрический
|
Происхождение и эволюция митоза[править | править код]

Возможные пути эволюции типов митоза у простейших. В квадратных скобках изображена гипотетическая промежуточная стадия. Условные обозначения: 1. Закрытый эвгленоидный митоз; 2. Закрытый внутриядерный плевромитоз; 3. Закрытый внеядерный плевромитоз; 4. Полузакрытый плевромитоз; 5. Закрытый внутриядерный ортомитоз; 6. Полузакрытый ортомитоз; 7. Открытый ортомитоз
Предполагается, что сложный митотический процесс высших организмов развивался постепенно из механизмов деления прокариот[111]. Это предположение подтверждается тем, что прокариоты появились приблизительно на миллиард лет раньше первых эукариот. Кроме того, в митозе эукариот и бинарном делении прокариот принимают участие схожие белки.
Возможные промежуточные стадии между бинарным делением и митозом можно проследить у одноклеточных эукариот, у которых в ходе деления не разрушается ядерная мембрана. У большинства же других эукариот, в том числе растений и животных, веретено деления формируется вне ядра, а ядерная оболочка разрушается в течение митоза. Хотя митоз у одноклеточных эукариот ещё недостаточно изучен, можно предположить, что он произошёл от бинарного деления и в конечном счёте достиг того уровня сложности, который имеется у многоклеточных организмов[112].
У многих простейших эукариот митоз также остался процессом, связанным с мембраной, однако теперь уже не плазматической, а ядерной[113]. Возможно, в связи с увеличением размера и числа хромосом, структура типа мезосомы разделилась на два элемента: ЦОМТ на ядерной оболочке и кинетохор на хромосоме. Для соединения данных структур между собой в процессе эволюции развилась промежуточная система микротрубочек. В рамках данного представления, наиболее древним и примитивным считается закрытый внутриядерный плевромитоз. Сегрегация хромосом при этом происходит путём расхождения ЦОМТ, к которым хромосомы крепятся посредством микротрубочек. В свою очередь, ЦОМТ закреплены на ядерной оболочке и расходятся за счёт роста ядерной мембраны между ними[114].
От разных вариантов закрытого внутриядерного плевромитоза, вероятно, берут своё начало несколько параллельных эволюционных линий[114]. В качестве эволюционно прогрессивных признаков при этом рассматриваются: распад ядерной оболочки во время митоза; переход ЦОМТ из ядра в цитоплазму; образование биполярного веретена; усиление спирализации хромосом; формирование экваториальной пластинки в метафазе. Таким образом, эволюция митотического деления идёт в направлении от закрытого внутриядерного плевромитоза к открытому ортомитозу[115].
Эндомитоз[править | править код]
Основная статья: Эндомитоз
Эндомитоз представляет собой разновидность митоза без деления ядра или клетки, в результате чего в клетке накапливается множество копий одних и тех же хромосом, собранных в одном ядре. Этот процесс может также включать эндоредупликацию, а клетки в этом случае называются эндоплоидными[116]. Примером клеток, подвергающихся эндомитозу, могут служить мегакариоциты, дающие начало тромбоцитам[117].
Крайним случаем эндомитоза является образование гигантских политенных хромосом, появляющихся как результат многократного воспроизведения хромосом без последующего расхождения. Такие хромосомы встречаются в слюнных железах некоторых насекомых, у личинок двукрылых в ядрах клеток кишечника и у некоторых растений в ядрах синергид (например, гороха)[118] .
Значение митоза[править | править код]
Митоз является важным средством поддержания постоянства хромосомного набора. В результате митоза осуществляется идентичное воспроизведение клетки. Следовательно, ключевая роль митоза — копирование генетической информации.
Митоз происходит в следующих случаях:
· Рост и развитие. Количество клеток в организме в процессе роста увеличивается благодаря митозу. Это лежит в развитии многоклеточного организма из единственной клетки — зиготы, а также роста многоклеточного организма.
· Перемещение клеток. В некоторых органах организма, например, коже и пищеварительном тракте, клетки постоянно отшелушиваются и заменяются новыми. Новые клетки образуются путём митоза, а потому являются точными копиями своих предшественников. Схожим путём происходит замена красных кровяных клеток — эритроцитов, имеющих короткую продолжительность жизни — 4 месяца, а новые эритроциты формируются путём митоза.
· Регенерация. Некоторые организмы способны восстанавливать утраченные части тела. В этих случаях образование новых клеток часто идёт путём митоза. Например, благодаря митозу морские звёзды восстанавливают утраченные лучи.
· Бесполое размножение. Некоторые организмы образуют генетически идентичное потомство путём бесполого размножения. Например, гидры размножаются бесполым способом при помощи почкования. Поверхностные клетки гидры подвергаются митозу и образуют скопления клеток, называемые почками. Митоз продолжается и в клетках почки, и она вырастает во взрослую особь. Сходное клеточное деление происходит при вегетативном размножении растений.
См. также[править | править код]
· Амитоз
· Анеуплоидия
· Мейоз
· Плоидность
· Политенные хромосомы
Примечания[править | править код]
Комментарии
↑ Показывать компактно
1. ↑ Сам факт разделения морфологии митотического веретена на два типа не отменяет возможности сочетания обоих в пределах одного организма. Например, в раннем эмбриогенезе млекопитающих при делении созревания ооцита и при I и II делении зиготы наблюдаются бесцентриолярные анастральные митозы. Но уже начиная с третьего клеточного деления и во всех последующих, клетки делятся при участии астральных веретен, в полюсах которых всегда обнаруживаются центриоли[25]
2. ↑ Первоначально, исходя из морфологических особенностей митоза, этот процесс был разделен лишь на четыре основные стадии: профазу, метафазу, анафазу и телофазу.[34]
3. ↑ Если митотические клетки поместить в тяжелую воду (D2O) или обработать таксолом (эти воздействия подавляют разборку микротрубочек), то нити веретена будут удлиняться. Такое стабилизированное веретено не может тянуть хромосомы, и митоз останавливается. Но митоз блокируется и при прямо противоположном воздействии, если нити веретена обратимо разрушить с помощью одного из трех агентов, подавляющих сборку тубулина в микротрубочки, – колхицина, низкой температуры или высокого гидростатического давления.[45]
4. ↑ Существует, как минимум, три гипотетические модели, объясняющие вероятный механизм расхождения хромосом в анафазе А. По одной из них перемещение хроматид объясняется наличием в кинетохоре «шагающих» белков, сходных по своей природе с динеином или кинезином; они продвигаются по микротрубочке, используя для этого энергию гидролиза АТФ. По другой гипотезе движение хромосом обусловлено распадом микротрубочек: по мере того как субъединицы тубулина диссоциируют, кинетохор, чтобы сохранить связь с микротрубочкой, должен скользить в направлении полюса. Третья возможность состоит в том, что микротрубочки не ответственны прямо за возникновение силы, движущей кинетохор к полюсам, а просто регулируют движение, вызываемое какой-то другой структурой.[59]
5. ↑ Существует целый ряд примеров, описывающих многократные митотические деления ядер без сопутствующего разделения клеточного тела. Так, в эндосперме многих растений протекают множественные митозы без деления цитоплазмы, что приводит к образованию многоядерного симпласта. Аналогичная ситуация наблюдается при синхронных делениях многочисленных ядер миксомицетов, или на ранних этапах развития зародышей некоторых насекомых.[66]
6. ↑ В качестве возможных рассматриваются несколько инициирующих моделей. Например, предполагается, что комплексы M-Cdk1 не полностью блокируются семейством ингибиторов Wee1. В результате, пропорционально увеличению концентрации митотических циклинов, к началу профазы может накопиться критическая масса активных киназ M-Cdk1. Частичная активация циклин-киназ у позвоночных, возможно, обеспечивается фосфатазой Cdc25B, уровень активности которой возрастает с поздней S-фазы и достигает максимума в профазе митоза. Однако было продемонстрировано, что мышиные клетки способны делиться в отсутствии данного стимула. Ещё одним возможным активатором может быть комплекс циклин A-Cdk, сохраняющий свою активность с начала S-фазы вплоть до конца прометафазы митоза.[81]
7. ↑ После инфицирования культур диплоидных клеток лёгкого человека вирусом Herpes simplex число патологических митозов (к-митозы, хромосомные аберрации) увеличивалось с 3 % в контроле до 40—60 % в инфицированной культуре.[93]
8. ↑ На примере эпителия гортани человека были получены данные об увеличении числа патологических митозов при раке. Если при хроническом воспалении и в папилломах «юношеского» типа количество патологических митозов всего в 2—2,5 раза превышало их число в нормальном эпителии, то при предраке количество патологических митозов составляло около 25 %, а при раке и атипическом папилломатозе с переходом в рак оно достигало 36—45 %.[94]
9. ↑ К таким признакам, например, относятся: поведение ядерной оболочки со всеми переходами от интактной, в разной степени фрагментированной до полностью распадающейся; неоднозначное поведение ядрышка от сохраняющегося до частично или полностью исчезающего; разная степень спирализации (или полное отсутствие таковой у динофлагеллат) и морфологической дифференциации хромосом; особенности расположения хромосом в метафазной пластинке; наличие кинетохоров и различия в их организации; различия в морфологии, характере заложения и организации веретена, продолжительность сохранения его межзональной зоны; появление наряду с центриолями особых полярных образований различной организации и места своей локализации; разная степень развития перинуклеарной оболочки и т. п.[108]
Стволовы́е кле́тки — недифференцированные (незрелые) клетки, имеющиеся у многих видов многоклеточных организмов. Стволовые клетки способны самообновляться, образуя новые стволовые клетки, делиться посредством митоза и дифференцироваться в специализированные клетки, то есть превращаться в клетки различных органов и тканей.
· 1909: Термин «стволовая клетка» (в оригинале «нем. Stammzelle») был предложен к широкому использованию 1 июня 1909 года на заседании гематологов в Берлине, где российско-американским гистологом Александром Максимовым методами своего времени были описаны гемопоэтические стволовые клетки в представленном докладе «Лимфоцит как общая стволовая клетка различных элементов крови в эмбриональном развитии и постфетальной жизни млекопитающих»[1]:
Мною теперь обнаружено, что эти примитивные кровяные клетки, как я их называю, никоим образом не являются эритробластами, как следовало бы по общепринятому представлению, а совершенно недифференцированными элементами с круглым светлым ядром и узкой базофильной протоплазмой; они не являются ни красными, ни белыми кровяными тельцами, хотя, скорее всего, их всё же можно было бы назвать белыми кровяными тельцами, поскольку они иногда, в особенности у цыплят, имеют амёбоидную форму и очень похожи на большие лимфоциты. Они далее размножаются, причем в первое время их число возрастает ещё и путём замены эндотелиальных клеток в примитивных сосудах
· 1970: Первые трансплантации аутологичных (своих собственных) стволовых клеток[2][3]. По некоторым сведениям, в 70-х годах престарелым членам Политбюро ЦК КПСС делали «прививки молодости» по 2-3 раза в год, инъецируя препараты стволовых клеток[4].
· 1978: в пуповинной крови обнаружены гемопоэтические стволовые клетки[5].
· 1981: эмбриональные клетки мыши получены из эмбриобласта (внутренней клеточной массы бластоцисты) учёными Мартином Эвансом, Мэттью Кауфманом и, независимо от них, Гэйл Р. Мартин. Введение в обиход термина «эмбриональная стволовая клетка» приписывается Гэйл Мартин.
· 1992: нейральные стволовые клетки получены in vitro. Разработаны протоколы их культивирования в виде нейросфер.
· 1997: Новым подходом к использованию стволовых клеток в терапии почечной недостаточности стала концепция применения «биоискусственной вспомогательной системы почечных канальцев» (Bioartifical renal tubule assist device, RAD). Это дополнение к «обычному» диализу: систему трубчатых мембран, внутренняя поверхность которых служит опорой для клеток ЭКП, дифференцированных из СК. Система дополняет аппарат «искусственная почка», — при этом кровь пациента фильтруется через мембраны, обмениваясь низкомолекулярными веществами с зафиксированными на них живыми клетками ЭПК[6][7].
· 1998: Джеймс Томсон и его сотрудники из Висконсинского университета в Мадисоне вывели первую линию человеческих ЭСК (эмбриональных стволовых клеток).
· 1999: журнал Science признал открытие эмбриональных стволовых клеток третьим по значимости событием в биологии после расшифровки двойной спирали ДНК и проекта «Геном человека».
· В 1999 году под руководством Humes H. D. была создана система, в которой использовались размноженные в течение нескольких пассажей, клетки эпителия проксимальных почечных канальцев поросят. Таким образом, использование «батареи» подобных катриджей может позволить достичь практически физиологической компенсации метаболической и эндокринной функции[8][9].
· 2005: перечень заболеваний, при лечении которых была успешно применена трансплантация стволовых клеток, достигает нескольких десятков. Основное внимание уделяется лечению злокачественных новообразований, различных форм лейкозов и других болезней крови. Появляются сообщения об успешной трансплантации стволовых клеток при заболеваниях сердечно-сосудистой и нервной систем. В различных исследовательских центрах проводятся исследования по применению стволовых клеток при лечении инфаркта миокарда и сердечной недостаточности. Разработаны международные протоколы лечения рассеянного склероза. Ищутся подходы к лечению инсульта, болезней Паркинсона и Альцгеймера.
· Август 2006: журнал Cell публикует исследование[10] Кадзутоси Такахаси и Синъя Яманака, посвящённое способу возвращения дифференцированных клеток в плюрипотентное состояние. Начинается эра индуцированных плюрипотентных стволовых клеток.
· Январь 2007: исследователи из Университета Уэйк Форест (Северная Каролина, США) под руководством доктора Энтони Атала из Гарварда сообщили[11] об открытии нового вида стволовых клеток, обнаруженных в амниотической жидкости (околоплодных водах). Они могут стать потенциальной заменой ЭСК в исследованиях и терапии.
· Июнь 2007: три независимые исследовательские группы сообщили, что зрелые клетки кожи мышей могут быть репрограммированы в состояние ЭСК. В том же месяце учёный Шухрат Миталипов заявил о создании линии стволовых клеток примата путём терапевтического клонирования.
· Ноябрь 2007: в журнале Cell опубликовано исследование Катсутоши Такагаши и Шинья Яманака «Индукция плюрипотентных стволовых клеток из фибробластов зрелого человека при определённых факторах»[12], а в журнале Science вышла статья «Индуцированные плюрипотентные стволовые клетки, выведенные из соматических клеток человека»[13] Джунинга Ю, в соавторстве с другими учёными из исследовательской группы Джеймса Томсона (англ.)русск.. Было доказано, что возможно индуцировать практически любую зрелую клетку человека и придать ей свойства стволовой, вследствие чего необходимость разрушения эмбрионов в лаборатории отпала, хотя предстоит определить риски канцерогенеза в связи с геном Мус и ретровирусным переносом генов.
· Январь 2008: Роберт Ланза и его коллеги из Advanced Cell Technology и Калифорнийского университета в Сан-Франциско вывели первые ЭСК человека без разрушения эмбриона[14].
· Январь 2008: посредством терапевтического клонирования культивированы клонированные бластоцисты человека.
· Февраль 2008: плюрипотентные стволовые клетки выведены из печени и желудка мыши, эти индуцированные клетки ближе к эмбриональным, чем индуцированные стволовые клетки, выведенные ранее и они не канцерогенны. Кроме того, гены, необходимые для индуцирования плюрипотентных клеток нет необходимости помещать в определённую область, что способствует развитию невирусных технологий репрограммирования клеток.
· Октябрь 2008: Сабина Конрад и её коллеги из Тюбингена (Германия) вывели плюрипотентные стволовые клетки из сперматогониальных клеток зрелого яичка человека путём культивирования in vitro с добавлением ФИЛ (фактора ингибирования (подавления) лейкемии).
· 30 октября 2008: эмбрионоподобные стволовые клетки выведены из человеческого волоса[15].
· Декабрь 2008: впервые опубликовано исследование врачей из Клиники регенеративной медицины Центено-Щульца (Centeno-Schultz Clinic), посвящённое успешной регенерации хряща в коленном суставе человека при использовании аутологичных зрелых МСК[16].
· 1 марта 2009: Андреаш Надь, Кэйсукэ Кадзи и их коллеги открыли способ выведения эмбрионоподобных стволовых клеток из обычных зрелых клеток с использованием инновационной технологии «обёртывания» для доставки специфических генов в клетки с целью репрограммирования без рисков, которые возникают при использовании вирусов. Помещение генов в клетку осуществляется при помощи электропорации.
· 28 мая 2009: Ким Гвансу и его коллеги из Гарварда заявили о том, что им удалось разработать способ манипулирования клетками кожи для выведения индуцированных плюрипотентных стволовых клеток с учётом индивидуальной специфики пациента, утверждая, что это «окончательное решение проблемы стволовых клеток».
· 2011: израильская исследовательница Инбар Фридрих Бен-Нун возглавила группу учёных, которая вывела первые стволовые клетки вымирающих видов животных[17]. Это прорыв, и благодаря ему можно спасти виды, которым грозит исчезновение[18].
· 2012: Введение пациентам стволовых клеток, взятых из их собственного костного мозга через три или семь дней после инфаркта миокарда, является хотя и безопасным, но неэффективным методом лечения — таковы результаты клинического исследования, проведённого при поддержке Национального института здоровья США. Однако исследования, проведённые немецкими специалистами в отделении кардиологии в Гамбурге, показали положительные результаты в лечении сердечной недостаточности, но не инфаркта миокарда.[19]
· 2012: Группа японских исследователей во главе с профессором Митинори Сайто из Университета Киото впервые в истории науки смогли вырастить яйцеклетки из стволовых клеток, оплодотворить их и добиться рождения здорового потомства у лабораторных мышей. 5 октября в электронном выпуске научного журнала Science они высказали предположение, что результаты их исследований внесут вклад в решение проблемы бесплодия.[20]
· 23 января 2013: та же группа Центра исследования и применения стволовых клеток Университета Киото вырастила из стволовых клеток ткани почек, надпочечников и половые клетки: были получены пять типов клеток почек, а также выращен фрагмент почечного канальца, участвующего в фильтрации крови.[21][22]
· 5 августа 2013: В результате многолетних опытов исследователей Маастрихтского университета на пути решения проблемы дефицита продовольствия в мире, создано мясо для стасорокаграммового гамбургера. Оно «сплетено» из 20 тысяч белковых волокон, выращенных за три месяца из коровьих стволовых клеток. В его производство инвестировано 250 000 евро[23][24].
· 2019: в Калифорнии генетики создали генную терапию в результате которой, стволовые клетки становятся «невидимыми» для иммунитета человека. Успешный опыт был проведён на «очеловеченных» мышах[25][26].
· Март 2020: Адам Кастильехо — второй человек в мире, который излечился от ВИЧ, путём пересадки стволовых клеток донорского костного мозга.
Свойства[править | править код]

Плюрипотентные эмбриональные стволовые клетки происходят как клетки внутренней клеточной массы (ICM) внутри бластоцисты. Эти стволовые клетки могут стать любой тканью организма, кроме плаценты. Только клетки более ранней стадии зародыша, известного как морула, являются тотипотентными, способными стать всеми тканями организма и внезародышевой плацентой.
Все стволовые клетки обладают двумя неотъемлемыми свойствами:
· Самообновление, то есть способность сохранять неизменный фенотип после деления (без дифференцировки).
· Потентность (дифференцирующий потенциал), или способность давать потомство в виде специализированных типов клеток.
Количество стволовых клеток у человека[править | править код]
· У новорождённого — 1:10.000[источник не указан 407 дней]
· У подростков — 1:100.000
· У взрослого — 1:1.000.000
· У пожилого — 1:100.000.000
Самообновление[править | править код]
Существуют два механизма, поддерживающих популяцию стволовых клеток в организме:
1. Асимметричное деление, при котором продуцируется одна и та же пара клеток (одна стволовая клетка и одна дифференцированная клетка[27]).
2. Стохастическое деление: одна стволовая клетка делится на две более специализированные.
Дифференцирующий потенциал[править | править код]
Классифицировали Вейгерс и Вейсман по способности продуцировать клеточные линии.
Дифференцирующий потенциал, или потентность, стволовых клеток — это способность производить определённое количество разных типов клеток. В соответствии с потентностью стволовые клетки делятся на следующие группы:
· Тотипотентные (омнипотентные) стволовые клетки могут дифференцироваться в клетки эмбриональных и экстраэмбриональных тканей, организованные в виде трёхмерных связанных структур (тканей, органов, систем органов, организма). Такие клетки могут дать начало полноценному жизнеспособному организму. К ним относится оплодотворённая яйцеклетка, или зигота. Клетки, образованные при первых нескольких циклах деления зиготы, также являются тотипотентными у большинства биологических видов. Однако к ним не относятся, например, круглые черви, зигота которых утрачивает тотипотентность при первом делении. У некоторых организмов дифференцированные клетки также могут обретать тотипотентность. Так, срезанную часть растения можно использовать для выращивания нового организма именно благодаря этому свойству.
· Плюрипотентные стволовые клетки являются потомками тотипотентных и могут давать начало практически всем тканям и органам, за исключением экстраэмбриональных тканей (например, плаценты). Из этих стволовых клеток развиваются три зародышевых листка: эктодерма, мезодерма и энтодерма. В 2015 году учёные обнаружили новый тип клеток — плюрипотентные стволовые клетки, специфичные к месту (region-selective pluripotent stem cells). Они самостоятельно колонизируют ту или иную область тела зародыша, после чего могут развиваться в клетки различных тканей[28].
· Мультипотентные стволовые клетки порождают клетки разных тканей, но многообразие их видов ограничено пределами одного зародышевого листка. Эктодерма даёт начало нервной системе, органам чувств, переднему и заднему отделам кишечной трубки, кожному эпителию. Из мезодермы формируются хрящевой и костный скелет, кровеносные сосуды, почки и мышцы. Из энтодермы — в зависимости от биологического вида — образуются различные органы, ответственные за дыхание и пищеварение. У человека это — слизистая оболочка кишечника, уротелий мочевого пузыря[29], а также печень, поджелудочная железа и лёгкие.
· Олигопотентные клетки могут дифференцироваться лишь в некоторые, близкие по свойствам, типы клеток. К ним, например, относятся клетки лимфоидного и миелоидного рядов, участвующие в процессе кроветворения.
· Унипотентные клетки (клетки-предшественницы, бластные клетки) — незрелые клетки, которые, строго говоря, уже не являются стволовыми, так как могут производить лишь один тип клеток. Они способны к многократному самовоспроизведению, что делает их долговременным источником клеток одного конкретного типа и отличает от не стволовых. Однако их способность к самовоспроизведению ограничена определённым количеством делений, что также отличает их от истинно стволовых клеток. К клеткам-предшественницам относятся, к примеру, некоторые из миосателлитоцитов, участвующих в образовании скелетной и мышечной тканей.
Классификация[править | править код]
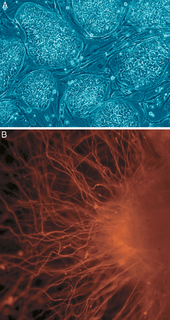
Человеческие эмбриональные стволовые клетки
A: Колонии стволовых клеток, которые ещё не дифференцированы.
B: Нервные клетки, пример типа клетки после дифференциации.
Стволовые клетки можно разделить на три основные группы в зависимости от источника их получения: эмбриональные, фетальные и постнатальные (стволовые клетки взрослого организма).
Эмбриональные стволовые клетки[править | править код]
Эмбриональные стволовые клетки (ЭСК) образуют внутреннюю клеточную массу (ВКМ), или эмбриобласт, на ранней стадии развития эмбриона. Они являются плюрипотентными.
|
|
|
© helpiks.su При использовании или копировании материалов прямая ссылка на сайт обязательна.
|